กรด-เบส
สารละลายอิเล็กโทรไลต์และนอนอิเล็กโทรไลต์
สารละลายอิเล็กโทรไลต์ คืออะไร อิเล็กโทรไลต์ (Electrolyte) หมายถึง สารที่ี่เมื่อละลายในน้ำจะนำไฟฟ้าได้ เนื่ื่องจากมีไอออนซึ่งอาจจะเป็นไอออนบวก หรือไอออนลบเคลื่อนที่ี่อยู่ในสารละลาย สารละลายอิเล็กโทรไลต์นี้ี้อาจเป็นสารละลายกรด เบส หรือเกลือก็ได้ ตัวอย่างเช่น สารละลายกรดเกลือ (HCl) สารละลายโซเดียมไฮดรอกไซด์ (NaOH) และสารละลายของเกลือ KNO3 เป็นต้น โดยในสารละลายดังกล่าวประกอบด้วยไอออน H+ , Cl- , OH- , K+
และ NO3 - ตามลำดับ
นอนอิเล็กโทรไลต์ (Non-electrolyte) หมายถึง สารที่ี่ไม่สามารถนำไฟฟ้าได้เมื่อละลายน้ำ ทั้งนี้เนื่องจาก สารพวกนอนอิเล็กโทรไลต์ จะไม่สามารถแตกตัวเป็นไอออนได้ เช่น น้ำบริสุทธิ์ น้ำตาล แอลกอฮอล์ เป็นต้น ความแตกต่างของสารอิเล็กโทรไลต์และนอน- อิเล็กโทรไลต์ พิจารณาจากสาร 2 ชนิด เมื่อละลายน้ำจะรวมกับน้ำเกิดการเปลี่ยนแปลง
อิเล็กโทรไลต์แก่และอิเล็กโทรไลต์อ่อน
สารละลายอิเล็กโทรไลต์ต่างๆ นำไฟฟ้าได้ไม่เท่ากัน เนื่ื่องจากการแตกตัวเป็นไอออนของอิเล็กโทรไลต์ไม่เท่ากัน อิเล็กโทรไลต์ที่ี่แตกตัวเป็นไอออนได้มากกว่า ก็จะนำไฟฟ้าได้ดีกว่าอิเล็กโทรไลต์ที่ี่แตกตัวเป็นไอออนได้น้อยกว่า อิเล็กโทรไลต์แบ่งออกได้เป็น 2 ประเภท ดังนี้ี้1. อิเล็กโทรไลต์แก่ (strong electrolyte) หมายถึง สารที่ี่ละลายน้ำแล้วแตกตัวเป็นไอออนได้มาก อาจจะแตกตัวได้ 100% และนำไฟฟ้าได้ดีมาก เช่น กรดแก่ และเบสแก่ และเกลือส่วนใหญ่จะแตกตัวได้ 100% เป็นต้น
2. อิเล็กโทรไลต์อ่อน (weak electrolyte) หมายถึง สารที่ละลายน้ำแล้วแตกตัวได้บางส่วน นำไฟฟ้าได้น้อย
ตารางตัวอย่างของอิเล็กโทรไลต์แก่ และอิเล็กโทรไลต์อ่อนบางชนิด
อิเล็กโทรไลต์แก่ (นำไฟฟ้าได้ดี) | อิเล็กโทรไลต์อ่อน (นำไฟฟ้าได้ไม่้ดี) |
เกลือที่ละลายนำ้ทั้งหมด H2SO4 HNO3 HCI HBr HCIO4 NaOH KOH Ca(OH)2 Ba(OH)2 | CH3COOH H2CO3 HNO2 H2SO3 H2S H2C2O4 H3BO3 HCIO NH4OH HF |
เราจะรู้ได้อย่างไรว่าสารละลายของเราเป็นสารละลายอิเล็กโทรไลต์หรือเปล่า?
การทดสอบว่าสารละลายเป็นสารละลายอิเล็กโทรไลต์ หรือไม่ก็ต้องดูการนำไฟฟ้าของสารละลาย เราอาจทดสอบโดยใช้เครื่องมือง่ายๆ ดังนี้ การทดสอบการนำไฟฟ้าของสารละลายสารละลายที่นำไฟฟ้า ได้แก่ สารละลายของกรด เบส และเกลือ อุปกรณ์ที่ใช้ในการทดลอง ประกอบด้วยขั้วไฟฟ้า 2 ขั้ว ต่อเข้ากับแหล่งให้พลังงานไฟฟ้า
( ให้ศักย์ไฟฟ้า) หลอดไฟ และสวิตซ์ให้ครบวงจรดังภาพ
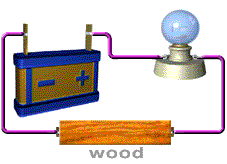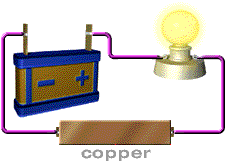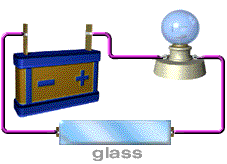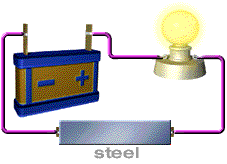
ภาพอุปกรณ์การวัดการนำไฟฟ้าของสารละลายอิเล็กโทรไลต์
ที่มา http://ssga.ru
ตัวอย่างผลการทดลองการทดสอบการนำไฟฟ้า
สารที่ใช้ทดสอบ | ผลการทดสอบ |
| น้ำบริสุทธิ์ น้ำที่มีน้ำตาลละลายอยู่ ยูเรีย CO(NH2)2 สารละลายเกลือ NaCl สารละลายเกลือ K2SO4 สารละลายกรด HCI สารละลายกรดแอซิติก CH3COOH สารละลายเบส NaOH สารละลายเบส Na4OH | ไม่นำไฟฟ้า (หลอดไฟไม่สว่าง) ไม่นำไฟฟ้า (หลอดไฟไม่สว่าง) ไม่นำไฟฟ้า (หลอดไฟไม่สว่าง) นำไฟฟ้า (หลอดไฟสว่าง) นำไฟฟ้า (หลอดไฟสว่าง) นำไฟฟ้า (หลอดไฟสว่าง) นำไฟฟ้าน้อย (หลอดไฟสว่าง) นำไฟฟ้า (หลอดไฟสว่าง) นำไฟฟ้า (หลอดไฟสว่าง) |
ผลที่ได้อธิบายได้ว่า สารละลายที่ี่ไม่มีไอออนอยู่ เช่น น้ำ หรือน้ำตาลทรายที่ี่ละลายอยู่ในน้ำมัน จะมีพันธะแบบโคเวเลนต์ ไม่สามารถแตกตัวเป็นไอออนได้ จึงไม่นำไฟฟ้า แต่ NaCl HCl เมื่ออยู่ในน้ำจะแตกตัวเป็น Na+ , Cl- หรือ H+ , Cl- ซึ่งเป็นไอออนที่เคลื่อนที่ี่ในสารละลายทำให้เกิดการนำไฟฟ้าขึ้นได้
จากการศึกษาสมบัติของสารละลาย พบว่า สารละลายกรดและสารละลายเบส เป็นสารละลายอิเล็กโทรไลต์ นำไฟฟ้าได้ เปลี่ยนสีกระดาษลิตมัส ทำปฏิกิริยากับโลหะและเกลือ กรดและเบสสามารถแตกตัวเป็นไอออน เมื่อเป็นสารละลาย เราจะศึกษาต่อไปถึงไอออนในสารละลายกรดและเบส ซึ่งทำให้สารละลายแสดงสมบัติเฉพาะตัวดังกล่าว
ไอออนในสารละลายกรด
ในสารละลายกรดทุกชนิด จะมีไอออนที่เหมือนกันอยู่ส่วนหนึ่งคือ H+ หรือ เมื่อรวมกับน้ำได้เป็น H3O+( ไฮโดรเนียมไอออน) ทำให้กรดมีสมบัติเหมือนกัน ตัวอย่างเช่น สารละลายกรดไฮโดรคลอริก (HCl) ซึ่งเกิดจากกรด HCl ละลายในน้ำ โมเลกุลของ HCl และ น้ำต่างก็เป็นโมเลกุลโคเวเลนต์มีขั้ว ทำให้เกิดแรงดึงดูดระหว่างขั้วของ HCl และน้ำ โดยที่โปรตอน (H+) ของ HCl ถูกดึงดูดโดยโมเลกุลของน้ำเกิดเป็นไฮโดรเนียมไอออน (H+ + H2O HCl (g) + H2O (l) H3O+ (aq) + Cl- (aq)
H3O+ (aq) + Cl- (aq)
ไฮโดรเนียมไอออนในน้ำไม่ได้อยู่เป็นไอออนเดียว แต่จะมีน้ำหลายโมเลกุลมาล้อมรอบอยู่ด้วย เช่น อาจอยู่ในรูปของ H5O2+, H7O3+ , H9O4+ เป็นต้นไอออนในสารละลายเบส
ในสารละลายเบสทุกชนิดจะมีไอออนที่ี่เหมือนกันอยู่คือ ไฮดรอกไซด์ไอออน ( OH-) ซึ่งทำให้เบสมีสมบัติเหมือนกัน และมีสมบัติต่างไปจากกรด ตัวอย่างเช่น เมื่อ NaOH ละลายน้ำจะแตกตัวได้ OH- ดังนี้
NaOH (s) 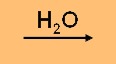 Na+(aq) + OH- (aq)
Na+(aq) + OH- (aq)
KOH (s) 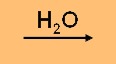 K+ (aq) + OH- (aq)
K+ (aq) + OH- (aq)
NH3 (g) + H2O (l)  NH4+ (aq) + OH-(aq)
NH4+ (aq) + OH-(aq)
ประโยชน์ของสารละลายกรดและเบสในชีวิตประจำวัน
สารละลายกรดและเบสมีบทบาทที่สำคัญในชีวิตประจำวัน ทั้งมีอยู่ในธรรมชาติและที่สังเคราะห์ขึ้นใช้ประโยชน์ในด้านต่างๆ เช่น ในด้านอาหาร อุตสาหกรรม การแพทย์ ตัวอย่างเช่น น้ำส้มสายชู น้ำส้ม น้ำมะนาว เหล่านี้ล้วนเป็นสารละลายกรด น้ำส้มสายชู ประกอบด้วยกรดแอซิติก น้ำส้มและน้ำมะนาวประกอบด้วยกรดซิตริก นอกจากนั้น ก็มีกรดคาร์บอนิกในน้ำโซดา กรดซัลฟิวริกในสารละลายที่อยู่ในแบตเตอรี่ สารละลายเบสที่คุ้นเคยในชีวิตประจำวันได้แก่ โซดาทำขนม (NaHCO3), หรือโซดาแอส (NaCO3), โซเดียมไฮดรอกไซด์ (NaOH) หรือโซดาไฟทฤษฎีกรด - เบส
ในการที่จะให้นิยามของกรด- เบส และในการจำแนกสารต่างๆ ว่าเป็นกรดหรือเบสนั้นได้มีนักวิทยาศาสตร์ ได้ศึกษาและตั้งทฤษฎีกรด- เบส ขึ้นหลายทฤษฎีด้วยกัน ทฤษฎีกรด- เบสที่สำคัญมีดังนี้
ทฤษฎีกรด- เบสของอาร์เรเนียส
อาร์เรเนียส เป็นนักวิทยาศาสตร์ชาวสวีเดน ได้ตั้งทฤษฎีกรด- เบส ในปี ค. ศ. 1887 ( พ. ศ. 2430) อาร์เรเนียสศึกษาสารที่ละลายน้ำ (Aqueous solution) และการนำไฟฟ้าของสารละลายนั้น เขาพบว่าสารอิเล็กโทรไลต์จะแตกตัวเป็นไอออน เมื่อละลายอยู่ในน้ำและให้นิยามกรดไว้ว่า“ กรด คือ สารที่เมื่อละลายน้ำแล้วแตกตัวให้ไฮโดรเจนไอออน” เช่น
HCl (g)
HClO4(l)
“ เบสคือ สารที่เมื่อละลายน้ำแล้วแตกตัวให้ไฮดรอกไซด์ไอออน” เช่น
NaOH (s)
KOH (s)
ข้อจำกัดของทฤษฎีกรด - เบส อาร์เรเนียส
- ทฤษฎีกรด- เบส อาร์เรเนียส จะเน้นเฉพาะการแตกตัวในน้ำ ให้เป็น H+ และ OH- ไม่รวมถึงตัวทำละลายอื่นๆ ทำให้อธิบายความเป็นกรด- เบสได้จำกัด
- สารที่ี่จะเป็นกรดได้ต้องมี H+ อยู่ในโมเลกุล และสารที่ี่จะเป็นเบสได้ก็ต้องมี OH- อยู่ในโมเลกุล
ทฤษฎีกรด- เบส ของเบรินสเตต- เลารี
โจฮันส์ นิโคลัส เบรินสเตต นักเคมีชาวเดนมาร์ก และ โทมัส มาร์ติน ลาวรี นักเคมีชาวอังกฤษ ได้ศึกษาการให้และรับโปรตอนของสาร เพื่อใช้ในการอธิบายและจำแนกกรด- เบสได้กว้างขึ้น และได้ตั้งทฤษฎีกรด- เบสขึ้นในปี ค. ศ.1923 ( พ. ศ.2466)กรด คือ สารที่ี่สามารถให้โปรตอนกับสารอื่นๆ ได้ (Proton donor)
เบส คือ สารที่ี่สามารถรับโปรตอนจากสารอื่นได้ (Proton acceptor)
พิจารณาตัวอย่างต่อไปนี้
1.
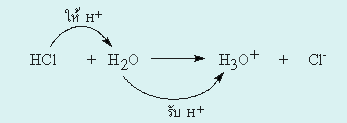
H2O เป็นสารที่ี่รับโปรตอน (H+) ดังนั้น H2Oจึงเป็นเบส
2.
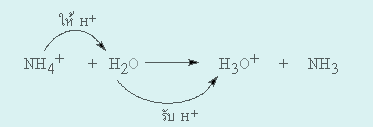
H2Oเป็นสารที่ี่รับโปรตอน (H+) ดังนั้น H2Oจึงเป็นเบส
ข้อจำกัดของทฤษฎีกรด - เบสของเบรินสเตต- ลาวรี
ทฤษฎีกรด- เบสของเบรินสเตต- ลาวรี ใช้อธิบายสมบัติของกรด- เบส ได้กว้างกว่าทฤษฎีของอาร์เรเนียส แต่ยังมีข้อจำกัดคือ สารที่จะทำหน้าที่เป็นกรดจะต้องมีโปรตอนอยู่ในสารนั้นสารที่เป็นได้ทั้งกรดและเบส
(Amphoteric)สารบางตัวทำหน้าที่เป็นทั้งกรด เมื่อทำปฏิกิริยากับสารตัวหนึ่ง และทำหน้าที่เป็นเบส เมื่อทำปฏิกิริยากับอีกสารหนึ่ง นั่นคือเป็นได้ทั้งกรดและเบส สารที่มีลักษณะนี้เรียกว่า สารเอมโพเทอริก(Amphoteric) เช่น H2O , HCO3- เป็นต้น
กรณีของ H2O

ดังนั้นอาจจะสรุปได้ว่า สารที่เป็นเอมโฟเทอริก ถ้าทำปฏิกิริยากับสารที่ให้โปรตอนได้ดีกว่า ตัวมันเองจะรับโปรตอน ( ทำหน้าที่เป็นเบส) แต่ถ้าไปทำปฏิกิริยากับสารที่ให้โปรตอนได้ไม่ดี ตัวมันเองจะเป็นตัวให้โปรตอนกับสารนั้น ( ทำหน้าเป็นกรด)
ทฤษฎีกรด- เบสของลิวอีส
ในปี ค. ศ. 1923 ( พ. ศ. 2466) ลิวอีสไดเสนอนิยามของกรดและเบสดังนี้กรด คือ สารที่สามารถรับอิเล็กตรอนคู่ จากเบส แล้วเกิดพันธะโคเวเลนต์
เบส คือ สารที่สามารถให้อิเล็กตรอนคู่ในการเกิดพันธะโคเวเลนต์
ปฏิกิริยาระหว่างกรด- เบส ตามทฤษฎีนี้ อธิบายในเทอมที่มีการใช้อิเล็กตรอนคู่ร่วมกัน กรดรับอิเล็กตรอนเรียกว่าเป็น Electrophile และเบสให้อิเล็กตรอนเรียกว่าเป็น Nucleophile และตามทฤษฎีนี้สารที่เป็นเบสต้องมีอิเล็กตรอนคู่อิสระ เช่น

ทฤษฎีของลิวอิสนี้มีข้อดีคือ สามารถจำแนกกรด- เบส ที่ไม่มีทั้ง H หรือ OH- ในสารนั้น และแม้ว่าสารนั้นไม่ได้อยู่ในรูปสารละลาย แต่อยู่ในสถานะแก๊สก็สามารถใช้ทฤษฎีลิวอิสอธิบายความเป็นกรดเบสได้
คู่กรด - เบส
จากปฏิกิริยาของกรดกับเบสที่กล่าวถึงแล้ว ตามทฤษฎีของเบรินสเตต- ลาวรี จะเห็นว่าในปฏิกิริยาหนึ่งๆ อาจจะจัดคู่กรด- เบสได้ 2 คู่ด้วยกัน ตัวอย่างเช่น
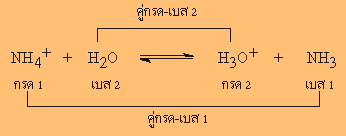
ปฏิกิริยาตัวอย่างนี้ ปฏิกิริยาไปข้างหน้า NH4+ ทำหน้าที่เป็นกรด เพราะให้ H+ กับ H2O แล้วได้เป็น NH3และ H2O รับ
H+ ทำหน้าที่เป็นเบส ส่วนปฏิกิริยาย้อนกลับ H3O+ เป็นกรด เพราะให้ H+ กับ NH3 ซึ่งเป็นเบส แล้วได้ H2O และ NH4+ ตามลำดับ
เรียก NH4+ ว่าคู่กรดของ NH3 ( เบส)
H2O ว่าคู่เบสของ H3O+ ( กรด)
NH3 ว่าคู่เบสของ NH4+ (กรด)
H3O+ ว่าคู่กรดของ H2O ( กรด)
จะเห็นได้ว่า คู่กรด- เบสนั้นจะมีจำนวนโปรตอน (H) ต่างกัน 1 ตัว หรืออาจกล่าวได้ว่า จำนวนโปรตอนของคู่กรด จะมากกว่าโปรตอนคู่เบสอยู่ 1 ตัวเสมอ
ตัวอย่าง คู่กรด - เบส
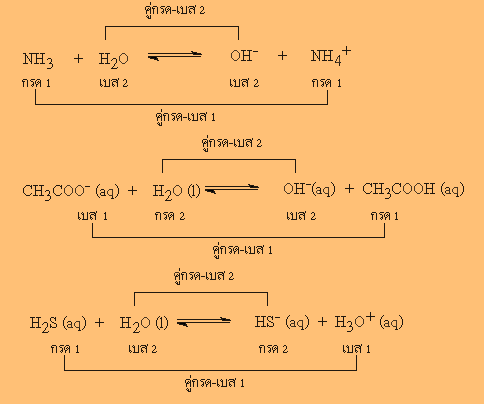
ความแรงของกรดและเบส
การเปรียบเทียบความแรงของกรดและเบส อาจจะพิจารณาได้ดังนี้
1. ดูจากการแตกตัวของกรด
กรดที่มีการแตกตัวมาก มีความเป็นกรดมาก กรดและเบสที่แตกตัวได้ 100% จะเรียกว่ากรดแก่ และเบสแก่ ตามลำดับ ซึ่งสามารถนำไฟฟ้าได้ดี แต่ถ้ากรดและเบสนั้นแตกตัวได้เพียงบางส่วนก็จะเรียกว่า กรดอ่อน หรือเบสอ่อน ตามลำดับ ซึ่งการนำไฟฟ้าจะไม่ดี
สำหรับการพิจารณาค่าการแตกตัวของกรดและเบสนั้น นอกจากจะคิดจากเปอร์เซ็นต์การแตกตัว หรืออาจจะดูได้จากค่าคงที่สมดุลของการแตกตัวของกรดหรือเบส (Ka หรือ Kb) เช่น
ความแรงของเบส พิจารณาจากค่า Kb กล่าวคือ ถ้ามีค่า Kb มาก มีความเป็นเบสมากกว่า Kb น้อย เช่น
NH3 Kb = 1.76 x 10-5
N2H4 Kb = 9.5 x 10-7
C 6H5NH2 Kb = 4.3 x 10 -10
ความเป็นเบส NH3> N2H4 > C6H5NH2
2. ดูจากความสามารถในการให้และรับโปรตอน
กรดแก่ ได้แก่ กรดที่ให้โปรตอนได้มาก
กรดอ่อน ได้แก่ กรดที่ให้โปรตอนได้น้อย
เบสแก่ ได้แก่ เบสที่รับโปรตอนได้มาก
เบสอ่อน ได้แก่ เบสที่รับโปรตอนได้น้อย
โดยมีข้อสังเกตเกี่ยวกับคู่กรด- เบส ดังนี้
- ถ้ากรดเป็นกรดแก่ คู่เบสจะเป็นเบสอ่อน เช่น
HCl (aq) + H2O
กรดแก่ เบสอ่อน
- ถ้ากรดเป็นกรดอ่อน คู่เบสจะเป็นเบสแก่ เช่น
กรดอ่อน เบสแก่
- ถ้าเบสเป็นเบสแก่ คู่กรดจะเป็น กรดอ่อน เช่น
เบสแก่ กรดอ่อน
- ถ้าเบสเป็นเบสอ่อน คู่กรดจะเป็น กรดแก่ เช่น
เบสอ่อน กรดแก่
ตารางลำดับความแรงของกรดและเบสตัวอย่างตามทฤษฎีของเบรินสเตต- ลาวรี

3. ดูจากการเรียงลำดับในตารางธาตุ
การพิจารณาความแรงของกรดและเบสดูจากการเรียงลำดับของธาตุที่อยู่ในกรดนั้้้น ตามตารางธาตุ ซึ่งแบ่งออกได้เป็น
3.1 กรดออกซี หมายถึง กรดที่ประกอบด้วย H, O และธาตุอื่นอีก เช่น HNO3 ,H3PO4,H3AsO4 ,HClO4 ถ้าจำนวนอะตอมออกซิเจนเท่ากัน ความแรงของกรดเรียงลำดับดังนี้
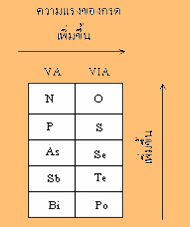
3.2 กรดที่ไม่มีออกซิเจน เช่น HCl, HBr, HF, และ HI ความแรงของกรดแรงลำดับดังนี้
HI > HBr > HCl > HF
H2S > H2O
การแตกตัวของกรดแก่และเบสแก่
การแตกตัวของกรดแก่และเบสแก่ จะแตกตัวได้หมด 100% หมายถึง การแตกตัวของกรดแก่และเบสแก่ เป็นไอออนได้หมดในตัวทำละลายซึ่งส่วนใหญ่เป็นน้ำ เช่น การแตกตัวของกรด HCl จะได้ H+ หรือ H3O+ และ Cl-ไม่มี HCl เหลืออยู่ หรือการแตกตัวของเบส เช่น NaOH ได้ Na+ และ OH- ไม่มี NaOH เหลืออยู่
การแตกตัวของกรดแก่และเบสแก่เขียนแทนด้วยลูกศร ซึ่งแสดงการเปลี่ี่ยนแปลงไปข้างหน้าเพียงอย่างเดียว เช่น
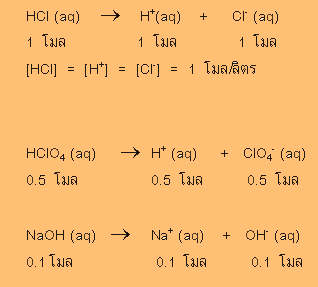
การคำนวณเกี่ยวกับการแตกตัวของกรดแก่และเบสแก่
ตัวอย่างที่ 1 จงคำนวณหา [H3O+] , [NO3-] ในสารละลาย 0.015 M HNO3
วิธีทำ
HNO3 +H2O
0.015
เพราะฉะนั้น [H3O+] = [NO3-] = 0.015 โมล/ ลิตร
ตัวอย่างที่ 2 ถ้า KOH 0.1 โมล ละลายน้ำและสารละลายมีปริมาตร 2 ลิตร ในสารละลายจะมีไอออนใดบ้างอย่างละกี่ี่โมลต่อลิตร
วิธีทำ
KOH (s)
0.1โมล/ 2 ลิตร
สารละลาย KOH 2 ลิตร มี KOH 0.1 โมล
สารละลาย KOH 1 ลิตร มี KOH
ดังนั้น KOH จะแตกตัวให้ K+ และ OH- อย่างละ 0.05 โมล/ ลิตร
ตัวอย่างที่ 3 สารละลายกรดแก่ (HA) 250 ลูกบาศก์เซนติเมตร มีปริมาณ H3O+ ไอออน 0.05 โมล สารละลายนี้ี้มีความเข้มข้นเท่าใด ถ้าเติมกรดนี้ี้ลงไปอีก 0.2 โมล โดยที่ี่สารละลายมีปริมาตรคงเดิม สารละลายที่ี่ได้จะมีความเข้มข้นเท่าใด
วิธีทำ
HA
0.05 โมล/ 250 cm3
สารละลาย HA 250 cm3 มี HA 0.05 โมล
สารละลาย HA 1000 cm3 มี HA =
เพราะฉะนั้นสารละลายที่ได้มีความเข้มข้น 0.20 โมล/ ลิตร
ถ้าเติมกรดอีก 0.2 โมล
สารละลายมี HA รวมทั้งหมด = 0.05 + 0.2 = 0.25 โมล
สารละลาย HA 250 cm3มี HA 0.25 โมล
สารละลาย HA 1000 cm3 มี HA =
เพราะฉะนั้นสารละลายที่ได้มีความเข้มข้น 1.00 โมล/ ลิตร
ตัวอย่างที่ 4 จงหาความเข้มข้นของ OH- ที่ี่เกิดจากการเอา NaOH 10.0 กรัม ละลายในน้ำทำเป็นสารละลาย 0.2 dm3 (Na = 23, O = 16, H = 1)
วิธีทำ
จำนวนโมลของ NaOH =
สารละลาย 0.2 dm3 มีเนื้อของ NaOH = 0.25 โมล
สารละลาย 1 dm 3มี NaOH =
เพราะฉะนั้นสารละลายมีความเข้มข้น 1.25 โมล/ ลิตร
และปฏิกิริยาการแตกตัวของ NaOH เป็นดังนี้
NaOH (aq)
1.25 โมล 1.25 โมล 1.25 โมล
เพราะฉะนั้นความเข้มข้นของ OH- = 1.25 โมล/ ลิตร
การแตกตัวของกรดอ่อน
สารละลายกรดอ่อน เช่น กรดแอซิติก (CH3COOH) เมื่อละลายน้ำ จะนำไฟฟ้าได้ไม่ดี ทั้งนี้ เพราะกรดแอซิติกแตกตัวเป็นไอออนได้เพียงบางส่วน เขียนแทนโดยสมการจะใช้ลูกศร
CH3COOH (aq) + H2O (l)
ปริมาณการแตกตัวของกรดอ่อน นิยมบอกเป็นร้อยละ เช่น กรด HA แตกตัวได้ร้อยละ 10 ในน้ำ หมายความว่า กรด HA 1 โมล เมื่อละลายน้ำ จะแตกตัวให้ H+
เพียง 0.10 โมล
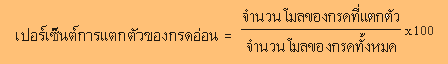
CH3COOH 1.0 M แตกตัวได้ 0.42 %
CH3COOH 0.10 M แตกตัวได้ 1.30 %
CH3COOH 0.010 M แตกตัวได้ 4.20 %
การแตกตัวของกรดมอนอโปรติก (monoprotic acid dissociation)
กรดมอนอโปรติก คือ กรดที่ี่แตกตัวให้ H+ ได้เพียง 1 ตัว เช่น HCOOH และ CH3COOH
HCOOH (aq)
CH3COOH (aq)
การแตกตัวของกรดพอลิโปรติก (polyprotic acid dissociation )
กรดพอลิโปรติก หมายถึง กรดที่ี่มีโปรตอนมากกว่า 1 ตัว และสามารถแตกตัวให้ H+ ได้มากกว่า 1 ตัว ถ้าแตกตัวได้ H+
2 ตัว เรียกว่า กรดไดโปรติก เช่น H2CO3 , H2S , H2C2O4 เป็นต้น
H2S
HS-
H2CO3
HCO3-
กรดที่ี่แตกตัวให้ H+ ได้ 3 ตัว เรียกว่า กรดไตรโปรติก เช่น H3PO4 , H3PO3
H3PO3
H2PO4-
HPO42-
ค่าคงที่สมดุลของกรดอ่อน (Ka)
กรดอ่อนแตกตัวได้เพียงบางส่วน ปฏิกิริยาการแตกตัวไปข้างหน้า และปฏิกิริยาย้อนกลับเกิดขึ้นได้พร้อมกัน และปฏิกิริยาการแตกตัวของกรดอ่อนนี้ี้จะอยู่ในภาวะสมดุล ค่าคงที่สมดุลนี้ี้จะหาได้ดังนี้

ตัวอย่างค่า Ka
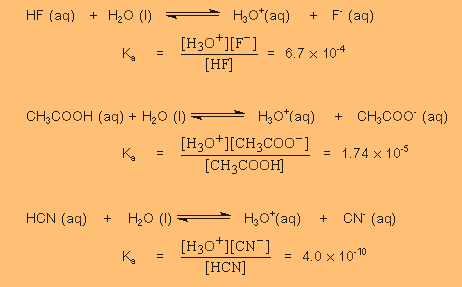
Ka (HF) > Ka (CH3COOH) > Ka (HCN)
เพราะฉะนั้นความแรงของกรด HF > CH3COOH > HCN
- กรณีกรดไดโปรติก

- กรณีกรดไตรโปรติก
 |
วิธีทำ HA (aq) + H2O (l)
เริ่มต้น 1 โมล/ ลิตร 0 0
ภาวะสมดุล 1 - 0.05 0.05 0.05 โมล/ ลิตร
 |
ตัวอย่างที่ 6 สารละลายกรด HA มีค่า Ka เป็น 6.8 x 10-4 สารละลายกรดนี้มีความเข้มข้น 1 โมล/ ลิตร สารละลายกรดนี้จะมีความเข้มข้นของ H3O+ เท่าใด
วิธีทำ HA (aq) + H2O (l) เริ่มต้น 1 0 0
ภาวะสมดุล 1 - x x x
 |
ตัวอย่างที่ 7 ที่ี่ 250C กรดแอซิติก (CH3COOH) เข้มข้น 0.1 โมล/ ลิตร แตกตัวได้ 1.34 % จงคำนวณหาความเข้มข้นของไฮโดรเนียมไอออน แอซิเตตไอออน และ Ka
วิธีทำ0.1 mol/dm3 CH3COOH แตกตัวได้ 1.34 % หมายความว่า
CH3COOH 100 mol/dm3แตกตัวได้ = 1.34 mol/dm3
CH3COOH 0.1 mol/dm3 แตกตัวได้ =
CH 3COOH + H3O
เริ่มต้น 0.1 0 0
ภาวะสมดุล 0.1- 0.00134 0.00134 0.00134
 |
ตัวอย่างที่ 8 จงคำนวณหาความเข้มข้นของ H+ , SO42- , และ HSO4-ของสารละลายกรด H2SO4 เข้มข้น 0.05 โมล/ ลิตร กำหนดค่า
Ka2 = 1.26 x 102-
วิธีทำKa2 = 1.26 x 102-
กรด H2SO4เป็นกรดแก่แตกตัวได้ 100 % ในขั้นที่ 1
H2SO4 (aq)
0.50 โมล/ ลิตร
ขั้นที่ 2 HSO4-(aq) แตกตัวให้ H+ และ SO42-(aq) ดังนี้
HSO4- (aq)
เริ่มต้น 0.50 0.50 0 ( ความเข้มข้นของ HSO4- และ H+ ได้จากการแตกตัวขั้นที่ี่1)
ภาวะสมดุล 0.50-x 0.50+x x
 |
NH3(aq) + H2O (l)
 |
- โมโนโปรติกเบส (monoprotic base) จะรับ H+ ได้ 1 ตัว และมีค่า Kb เพียงค่าเดียว เช่น NH3
- โพลิโปรติกเบส (polyprotic base) จะรับ H+ ได้มากกว่า 1 ตัว และมีค่า Kb ได้หลายค่า เช่น ไฮดราซีน H2NNH2
H2NNH3+ + H2O
ตารางที่ 1ค่าคงที่สมดุลของเบสอ่อนบางตัว
 |
นอกจาก การบอกปริมาณการแตกตัวของเบสอ่อน ในลักษณะของค่า Kb แล้วก็ยังสามารถบอกปริมาณการแตกตัวของเบสอ่อนได้ในลักษณะของเปอร์เซ็นต์ของการแตกตัว ดังนี้
 |
ตัวอย่างการคำนวณ
ตัวอย่างที่ 9 จงเขียนค่าคงที่สมดุลของเบสอ่อนต่อไปนี้ C6H5NH2 , N2H2วิธีทำ
 |
วิธีทำ
 |
วิธีทำ
 |
วิธีทำ
 |

การแตกตัวของน้ำบริสุทธิ์ิิ์เป็นอย่างไร
น้ำเป็นอิเล็กโทรไลต์ที่ี่อ่อนมาก แตกตัวได้น้อยมาก ดังนั้น การนำไฟฟ้าของน้ำจะน้อย จนไม่สามารถตรวจสอบได้ด้วยการนำไฟฟ้าผ่านหลอดไฟ แต่ตรวจได้ด้วยเครื่องวัดกระแส (เป็นแอมมิเตอร์) อาจอนุโลมได้ว่าน้ำบริสุทธิ์เป็นสารนอนอิเล็กโทรไลต์
ตัวอย่างการวัดการนำไฟฟ้าของน้ำชนิดต่างๆ ได้แก่ น้ำกลั่นที่ี่อุณหภูมิห้อง น้ำกลั่นที่ี่อุณหภูมิ 60 - 70 องศาเซลเซียส น้ำคลอง น้ำประปา และน้ำฝน จะได้ผลดังตาราง
ตารางตัวอย่างการนำไฟฟ้าของน้ำชนิดต่างๆ
น้ำชนิดต่าง ๆ | เครื่องตรวจการนำไฟฟ้า | วัดด้วยแอมมิเตอร์ |
| น้ำกลั่นที่อุณหภูมิห้อง น้ำกลั่นที่อุณหภูมิ 60-70 0C น้ำคลอง น้ำประปา น้ำฝน | หลอดไฟไม่สว่าง หลอดไฟไม่สว่าง หลอดไฟไม่สว่าง หลอดไฟไม่สว่าง หลอดไฟไม่สว่าง | 40 80 90 85 80 |
ตามทฤษฎีของเบรินสเตตและลาวรี น้ำทำหน้าที่ี่เป็นทั้งกรดและเบส ไอออนที่ี่เกิดขึ้นจากการแตกตัวของน้ำ และมีการถ่ายเทโปรตอนกันเองได้ ( ออโตไอออนไนเซชัน)
 |
โมเลกุลของน้ำที่ี่เสีย H+ จะเปลี่ยนเป็น OH- ซึ่งมีประจุลบและโมเลกุลของน้ำที่ได้รับ H+ จะเปลี่ยนเป็น H3O+ ซึ่งมีประจุบวก เราอาจเขียนสมการกรด- เบส ได้ง่ายๆ ดังนี้
H2O (l) + H2O (l) เนื่องจากระบบนี้อยู่ในภาวะสมดุล สามารถเขียนสมการค่าคงที่สมดุลของ H2O ได้ดังนี้
 |
Kw คือค่าคงที่การแตกตัวของน้ำ มีค่าเท่ากับ 1 x 10-14ที่ 250C เนื่องจากน้ำบริสุทธิ์แตกตัวเป็นไอออนจะให้ความเข้มข้นของ H3O+ และ OH- เท่ากัน
 |
ดังนั้น น้ำบริสุทธิ์จึงมีสภาพเป็นกลางเนื่องจากปริมาณ H3O+ เท่ากับ OH- ค่าคงที่ี่สมดุลของน้ำมีค่าเปลี่ยนแปลงตามอุณหภูมิ แสดงดังตารางต่อไปนี้
ตารางค่า Kw ของน้ำที่ี่อุณหภูมิต่างๆ
อุณหภูมิ(0C) | Kw |
0 10 20 25 30 40 50 60 | 0.114 x 10-14 0.296 x 10-14 0.681 x 10-14 1.010 x 10-14 1.470 x 10-14 2.920 x 10-14 5.470 x 10-14 9.610 x 10-14 |
เราสามารถบอกความเป็นกรดเป็นเบสของสารละลายโดยค่า pH
pH ย่อมาจากคำว่า positive potential of the hydrogen ions คือ ค่าที่แสดงถึงความเข้มข้นของไฮโดรเจนไอออน (H+) หรือไฮโดรเนียมไอออน (H3O+) ใช้บอกความเป็นกรดหรือเบสของสารละลาย โดยค่า pH ของสารละลายเป็นค่าลอการิทึมของความเข้มข้นของไฮโดรเจนไอออน pH = -log [H3O+]
หรือ [H3O] + = 10-pH โดยที่ [H3O+] คือ ความเข้มข้นของ H3O+ หรือ H+ เป็นโมล/ลิตร
น้ำบริสุทธิ์ ที่อุณหภูมิ 25 0C จะมี [H3O+] = 1 x 10 -7 โมล/ลิตร
ดังนั้น pH = -log [H3O+] = -log [1 x 10 -7] = 7
นั่นคือ pH ของน้ำบริสุทธิ์ ที่อุณหภูมิ 25 0C เท่ากับ 7 ถือว่ามีสภาพเป็นกลาง คือไม่มีความเป็นกรดหรือเบส
ถ้า [H3O+] = 1 x 10 -5 ; pH = -log [H3O+] = -log [1 x 10 -5] = 5 (เป็นกรด)
ถ้า [H3O+] = 1 x 10 -9 ; pH = -log [H3O+] = -log [1 x 10 -9] = 9 (เป็นเบส)
ดังนั้นสรุปว่า
pH < 7 สารละลายเป็นกรด
pH = 7 สารละลายเป็นกลาง
pH > 7 สารละลายเป็นเบส
หรืออาจจะเขียนเป็นสเกลได้ดังนี้
หรือ [H3O] + = 10-pH โดยที่ [H3O+] คือ ความเข้มข้นของ H3O+ หรือ H+ เป็นโมล/ลิตร
น้ำบริสุทธิ์ ที่อุณหภูมิ 25 0C จะมี [H3O+] = 1 x 10 -7 โมล/ลิตร
ดังนั้น pH = -log [H3O+] = -log [1 x 10 -7] = 7
นั่นคือ pH ของน้ำบริสุทธิ์ ที่อุณหภูมิ 25 0C เท่ากับ 7 ถือว่ามีสภาพเป็นกลาง คือไม่มีความเป็นกรดหรือเบส
ถ้า [H3O+] = 1 x 10 -5 ; pH = -log [H3O+] = -log [1 x 10 -5] = 5 (เป็นกรด)
ถ้า [H3O+] = 1 x 10 -9 ; pH = -log [H3O+] = -log [1 x 10 -9] = 9 (เป็นเบส)
ดังนั้นสรุปว่า
pH < 7 สารละลายเป็นกรด
pH = 7 สารละลายเป็นกลาง
pH > 7 สารละลายเป็นเบส
หรืออาจจะเขียนเป็นสเกลได้ดังนี้
 |
นอกจากจะบอกความเป็นกรดเป็นเบสของสารละลายด้วยค่า pH แล้วยังสามารถบอกค่าความเป็นกรด-เบส ได้โดยใช้ค่า pOHp ของสารละลาย คือ ค่าที่บอกความเข้มข้นของ OH-
pOH = -log[OH- ]โดย pH + pOH = 14
ตารางแสดง สเกล pH ของสารละลายที่มีความเข้มข้นต่างๆ กัน
 |
วิธีวัด pH ของสารละลายวัดได้ 2 วิธี ดังนี้
1. วิธีเปรียบเทียบสี วิธีนี้เป็นการวัด pH โดยประมาณ (มีความถูกต้อง 0.5 หน่วย pH) ซึ่งทำได้โดยเติมอินดิเคเตอร์ที่เหมาะสมลงไปในสารละลายที่ต้องการวัด pH แล้วเปรียบเทียบกับสารละลาย ทำได้โดยเติมอินดิเคเตอร์ที่เหมาะสมลงไปในสารละลายที่ต้องการวัด pH แล้วเปรียบเทียบสีกับสารละลายบัฟเฟอร์ที่ทราบค่า pH แน่นอน ซึ่งได้เติมอินดิเคเตอร์ชนิดเดียวกันไปแล้ว หรือใช้กระดาษชุบอินดิเคเตอร์ (กระดาษ pH) จุ่มลงไปแล้วเปรียบเทียบกับสีมาตรฐาน
2. วิธีวัดความต่างศักย์ วิธีนี้วัด pH ได้อย่างละเอียด (มีความถูกต้อง 0.01 หน่วย pH) โดยการใช้เครื่องมือที่เรียกว่า พีเอชมิเตอร์ ซึ่งวัด pH ของสารละลายได้โดยการวัดความต่างศักย์ระหว่างขั้วไฟฟ้า 2 ขั้ว
2. วิธีวัดความต่างศักย์ วิธีนี้วัด pH ได้อย่างละเอียด (มีความถูกต้อง 0.01 หน่วย pH) โดยการใช้เครื่องมือที่เรียกว่า พีเอชมิเตอร์ ซึ่งวัด pH ของสารละลายได้โดยการวัดความต่างศักย์ระหว่างขั้วไฟฟ้า 2 ขั้ว
ตัวอย่างที่ 1ให้หาค่า pH ของสารละลายที่มี H3 O+ เท่ากับ 1 x 10 -11 และ 6 x 10 -14 โมล/ลิตร
วิธีทำ
[ H3 O+] = 1 x 10-11
pH = -log[ H3 O+] = -log[1 x 10-11 ] = 11
[ H3 O+] = 6 x 10-4
pH = -log[ H3 O+] = -log[6 x 10-4 ] = 4 - log6 = 4 - 0.78 = 3.22
ตัวอย่างที่ 2 จงหา pH ของสารละลายที่มีความเข้มข้นของ H3 O+ = 4.8 x 10-13โมล/ลิตร
วิธีทำ pH = -log[ H3 O+]
= -log[4.8 x 10-13]
= 13 - log 4.8
= 12.32
ตัวอย่างที่ 3 สารละลายชนิดหนึ่งมี pH = 4.00 จะมีความเข้มข้นของไฮโดรเนียมไอออนเป็นเท่าใด
วิธีทำ pH = -log[ H3 O+]
4 = -log[ H3 O+]
[ H3 O+] = 10-4
= 1 x 10-4
ตัวอย่างที่ 4 จงคำนวณหา [H+ ], [OH- ] , pH , และ pOH ของสารละลายที่มีกรดแก่ HX 0.01 โมลในน้ำ 500 cm3
วิธีทำ
กรดแก่ HX แตกตัวได้ 100 %
[HX] = 0.1 โมล/ลิตร = 0.02 โมล/ลิตร
HX
0.02 โมล/ลิตร 0.02 โมล/ลิตร
เพราะฉะนั้น [H+] = 0.02 โมล/ลิตร
จาก [H+][OH- ] = 1 x 10-14 โมล/ลิตร
[OH- ] = = 5.0 x 10 --13
เพราะฉะนั้น [OH- ] = 5.0 x 10--13 โมล/ลิตร
pH = -log[H+] = -log(0.02) = 1.70
pH + pOH = 14
pOH = 14 - pH = 14 - 1.70 = 12.30
อินดิเคเตอร์สำหรับกรด-เบส และการเปลี่ยนสีของอินดิเคเตอร์
อินดิเคเตอร์สำหรับกรด-เบส คืออะไร
อินดิเคเตอร์ คือ สารที่ใช้บอกความเป็นกรด-เบส ของสารละลายได้อย่างหนึ่ง สารประกอบที่เปลี่ยนสีได้ที่ pH เฉพาะตัว จะถูกนำมาใช้เป็นอินดิเคเตอร์ได้ เช่น ฟีนอล์ฟทาลีน จะไม่มีสีเมื่ออยู่ในสารละลายกรด และจะเปลี่ยนเป็นสีชมพู เมื่ออยู่ในสารละลายเบสที่มี pH 8.3 |
ภาพฟีนอล์ฟทาลีน
อินดิเคเตอร์สำหรับกรด-เบส เป็นสารอินทรีย์ อาจเป็นกรดหรือเบสอ่อนๆ ซึ่งสามารถเปลี่ยนจากรูปหนึ่งไปเป็นอีกรูปหนึ่งได้ เมื่อ pH ของสารละลายเปลี่ยน
การเปลี่ยนสีของอินดิเคเตอร์
HIn เป็นสัญลักษณ์ของอินดิเคเตอร์ที่อยู่ในรูปกรด (Acid form)
In- เป็นสัญลักษณ์ของอินดิเคเตอร์ที่อยู่ในรูปเบส (Basic form)
รูปกรดและรูปเบสมีภาวะสมดุล เขียนแสดงได้ด้วยสมการ ดังนี้
HIn (aq) + H2O (l)In- เป็นสัญลักษณ์ของอินดิเคเตอร์ที่อยู่ในรูปเบส (Basic form)
รูปกรดและรูปเบสมีภาวะสมดุล เขียนแสดงได้ด้วยสมการ ดังนี้
ไม่มีสี * สีชมพู* ; (* = กรณีเป็นฟีนอล์ฟทาลีน)
(รูปกรด) (รูปเบส)
| Kind = | 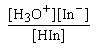 |
HIn และ In- มีสีต่างกันและปริมาณต่างกัน จึงทำให้สีของสารละลายเปลี่ยนแปลงได้ ถ้าปริมาณ HInมากก็จะมีสีของรูปกรด ถ้ามีปริมาณ In-มากก็จะมีสีของรูปเบส การที่จะมีปริมาณ HIn หรือ In มากกว่าหรือน้อยกว่านั้นขึ้นอยู่กับปริมาณ H3O+ ในสารละลาย ถ้ามี H3O+ มากก็จะรวมกับ In- ได้เป็น HIn ได้มากจะเห็นสารละลายใสไม่มีสีของ HIn แต่ถ้าอยู่ในสารละลายที่มี OH- มาก OH-จะทำปฏิกิริยากับ H3O+ ทำให้H3O+ ลดลง ซึ่งจะมีผลทำให้เกิดปฏิกิริยาไปข้างหน้าได้ In- มากขึ้น จะเห็นสารละลายในรูปของ In- คือเห็นเป็นสีชมพู
ช่วง pH ที่อินดิเคเตอร์เปลี่ยนสีจากรูปหนึ่งไปเป็นอีกรูปหนึ่ง สารละลายจะมีสีผสมระหว่างรูปกรดและรูปเบส เรียกว่า ช่วง pH ของอินดิเคเตอร์ (pH range หรือ pH interval)
ช่วง pH ของอินดิเคเตอร์หาได้จากค่า Kind ของอินดิเคเตอร์ดังนี้
HIn (aq) + H2O (l)ช่วง pH ที่อินดิเคเตอร์เปลี่ยนสีจากรูปหนึ่งไปเป็นอีกรูปหนึ่ง สารละลายจะมีสีผสมระหว่างรูปกรดและรูปเบส เรียกว่า ช่วง pH ของอินดิเคเตอร์ (pH range หรือ pH interval)
ช่วง pH ของอินดิเคเตอร์หาได้จากค่า Kind ของอินดิเคเตอร์ดังนี้
ไม่มีสี * (รูปกรด) สีชมพู* (รูปเบส) ; (* = กรณีเป็นฟีนอล์ฟทาลีน)
| Kind = | 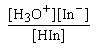 |
| [H3O+] = Kind |
| -log [H3O+] = -logKind |
| pH = pKind |
| - จะเริ่มเห็นสีของรูปกรดเมื่อ |
pH = pKind- 1
| - จะเริ่มเห็นสีของรูปเบสเมื่อ |
| pH = pKind - log |
นั่นคือ ช่วง pH ของอินดิเคเตอร์ = pKind
ตัวอย่างเช่น เมทิลเรด มีช่วง pH 4.4 - 6.2 หมายความว่า สารละลายที่หยดเมทิลเรดลงไป จะเปลี่ยนสีจากรูปกรด (แดง) ไปเป็นรูปเบส (เหลือง) ในช่วง pH ตั้งแต่ 4.4 - 6.2 นั่นคือ
- ถ้า pH < 4.4 จะให้สีแดง (รูปกรด)
- pH อยู่ระหว่าง 4.4 - 6.2 จะให้สีผสมระหว่างสีแดงกับเหลือง คือ สีส้ม
- pH > 6.2 จะให้สีเหลือง (รูปเบส)
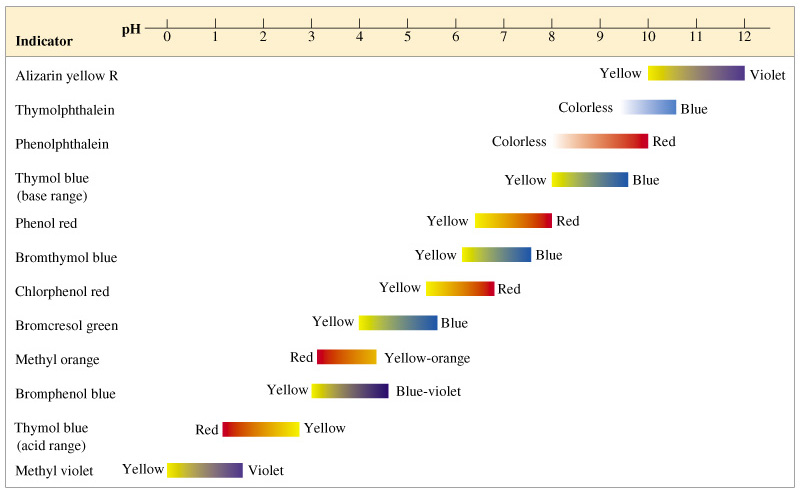 |
ภาพแสดงสีของอินดิเคเตอร์แต่ละชนิด
อย่างไรก็ตาม อินดิเคเตอร์ชนิดหนึ่งๆ จะใช้หาค่า pH ของสารละลายได้อย่างคร่าวๆ เท่านั้น เช่น เมื่อนำสารละลายมาเติม เมทิลออเรนจ์ลงไป (ช่วง pH ของเมทิลออเรนจ์เท่ากับ 3.0 - 4.4 และสีที่เปลี่ยนอยู่ในช่วง สีแดง
ตัวอย่าง การทดลองหาค่า pH ของสารละลายชนิดหนึ่ง โดยใช้อินดิเคเตอร์ 5 ชนิดด้วยกัน ผลการทดลองเป็นดังนี้
ชนิดของอินดิเคเตอร์ | ช่วง pH | สีที่เปลี่ยน | สีสารละลายที่ได้จากการทดลอง |
| 1. methyl yellow 2. Bromeresol green 3. Methyl red 4. Bromothymol blue 5. Phenophtalein | 2.9-4.0 3.8-5.4 4.4-6.2 6.0-7.6 8.0-9.6 | สีแดง-เหลือง เหลือง-น้ำเงิน แดง-เหลือง เหลือง-น้ำเงิน ไม่มีสี-สีชมพู | เหลือง น้ำเงิน ส้ม เหลือง ไม่มีสี |
ให้หาค่า pH ของสารละลายจากข้อมูลการทดลองข้างต้น
แนวคิด จากอินดิเคเตอร์ชนิดที่ 1 แสดงว่า pH ของสารละลาย > 4 จากอินดิเคเตอร์ชนิดที่ 2 แสดงว่า pH ของสารละลายอยู่ระหว่าง 4.4-6.2 จากอินดิเคเตอร์ชนิดที่ 3 แสดงว่า pH ของสารละลาย > 5.4 จากอินดิเคเตอร์ชนิดที่ 4 แสดงว่า pH ของสารละลาย < 6 จากอินดิเคเตอร์ชนิดที่ 5 แสดงว่า pH ของสารละลาย < 8.0 สรุปได้ว่า สารละลายมี pH อยู่ระหว่าง 5.4 - 6
การหา pH ของสารละลายโดยใช้อินดิเคเตอร์หลายๆ ชนิดนี้ ไม่สะดวกในการใช้ จึงมีการคิดที่จะนำอินดิเคเตอร์หลายๆ ชนิด ซึ่งเปลี่ยนสีในช่วง pH ต่างๆ กันมาผสมกันในสัดส่วนที่เหมาะสม จะสามารถใช้บอกค่า pH ของสารละลายได้ละเอียดขึ้น อินดิเคเตอร์ผสมนี้เรียกว่า ยูนิเวอร์ซัลอินดิเคเตอร์ ซึ่งสามารถเปลี่ยนสีได้ในสารละลายที่มี pH ต่างๆ กันเกือบทุกค่า
การใช้ยูนิเวอร์ซัลอินดิเคเตอร์ หยดยูนิเวอร์ซัลอินดิเคเตอร์ลงในสารละลายที่ต้องการหาค่า pH ประมาณ 3 หยดต่อสารละลาย 3 cm3 สังเกตสีของสารละลายแล้วเปรียบเทียบกับสีมาตรฐานของยูนิเวอร์ซัลอินดิเคเตอร์ที่ pH ต่างๆ ว่าสีของสารละลายตรงกับสีมาตรฐานที่ pH ใด ก็จะมีค่าเท่ากับ pH นั้น
แนวคิด จากอินดิเคเตอร์ชนิดที่ 1 แสดงว่า pH ของสารละลาย > 4 จากอินดิเคเตอร์ชนิดที่ 2 แสดงว่า pH ของสารละลายอยู่ระหว่าง 4.4-6.2 จากอินดิเคเตอร์ชนิดที่ 3 แสดงว่า pH ของสารละลาย > 5.4 จากอินดิเคเตอร์ชนิดที่ 4 แสดงว่า pH ของสารละลาย < 6 จากอินดิเคเตอร์ชนิดที่ 5 แสดงว่า pH ของสารละลาย < 8.0 สรุปได้ว่า สารละลายมี pH อยู่ระหว่าง 5.4 - 6
การหา pH ของสารละลายโดยใช้อินดิเคเตอร์หลายๆ ชนิดนี้ ไม่สะดวกในการใช้ จึงมีการคิดที่จะนำอินดิเคเตอร์หลายๆ ชนิด ซึ่งเปลี่ยนสีในช่วง pH ต่างๆ กันมาผสมกันในสัดส่วนที่เหมาะสม จะสามารถใช้บอกค่า pH ของสารละลายได้ละเอียดขึ้น อินดิเคเตอร์ผสมนี้เรียกว่า ยูนิเวอร์ซัลอินดิเคเตอร์ ซึ่งสามารถเปลี่ยนสีได้ในสารละลายที่มี pH ต่างๆ กันเกือบทุกค่า
การใช้ยูนิเวอร์ซัลอินดิเคเตอร์ หยดยูนิเวอร์ซัลอินดิเคเตอร์ลงในสารละลายที่ต้องการหาค่า pH ประมาณ 3 หยดต่อสารละลาย 3 cm3 สังเกตสีของสารละลายแล้วเปรียบเทียบกับสีมาตรฐานของยูนิเวอร์ซัลอินดิเคเตอร์ที่ pH ต่างๆ ว่าสีของสารละลายตรงกับสีมาตรฐานที่ pH ใด ก็จะมีค่าเท่ากับ pH นั้น
pH สารละลาย | สี |
3 | แดง |
4 | ส้มแดง |
5 | ส้ม |
6 | ส้มเหลือง |
7 | เหลืองเขียว |
8 | เขียว |
9 | น้ำเงินเขียว |
10 | ม่วง |
11 | ม่วงแดง |
สารละลายกรด-เบส ในชีวิตประจำวัน และฝนกรด (Acid rain)
สารละลายกรด-เบส ในชีวิตประจำวัน
ค่า pH ของสารละลายในสิ่งมีชีวิตมีค่าเฉพาะตัว เช่น pH ของเอนไซม์ในกระเพาะอาหารมีค่าประมาณ 1.5 pH ของเลือดและน้ำลาย มีค่าเท่ากับ 7.4 และ 6.8 ตามลำดับสาร | ช่วง pH |
| น้ำย่อยในกระเพาะอาหาร ปัสสาวะ น้ำลาย เลือด น้ำดี | 1.6-2.5 5.5-7.0 6.2-7.4 7.35-7.45 7.8-8.6 |
ฝนกรด (Acid rain)
น้ำฝนที่มี pH ประมาณ 5.6 - 6.0 ซึ่งมีภาวะเป็นกรดอ่อนๆ ปัจจุบันในประเทศอุตสาหกรรม pH ของน้ำฝนมีค่าต่ำกว่า 5.6 ทั้งนี้เนื่องจากมีการเผาไหม้เชื้อเพลิง เช่น ถ่านหิน น้ำมัน เป็นต้น ซึ่งเชื้อเพลิงเหล่านี้มีสารซัลเฟอร์ (S) อยู่ ทำให้เกิดแก๊ส SO2 ซึ่งเมื่อถูกปล่อยออกมาสู่บรรยากาศ และละลายในน้ำ หรือถูกออกซิไดส์ต่อเป็น SO3 แล้วละลายในน้ำฝนได้กรด H2SO4 แล้วจะไปเพิ่มความเป็นกรดให้กับน้ำฝน ซึ่งอาจจะทำให้ pH ต่ำกว่า 3 ในบริเวณที่มีสภาพแวดล้อมไม่ดี SO3 (g) + H2O (l)  H2SO4 (aq)
H2SO4 (aq)
ผลที่เกิดขึ้นคือ ฝนกรดจะไปทำลายต้นไม้ ทำลายชีวิตสัตว์น้ำ ทำให้โลหะเกิดการผุกร่อน หินถูกกัดเซาะ เป็นต้นSO2 อาจจะรวมกับน้ำได้เป็น H2SO3 และนอกจากสารประกอบของซัลเฟอร์แล้วก็อาจมีสารประกอบของ N ซึ่งจะถูกเปลี่ยนเป็น NO2, HNO2 และ HNO3 ได้เช่นกัน ซึ่งเมื่อละลายในน้ำฝนก็จะไปเพิ่มความเป็นกรดให้กับน้ำฝนได้ ปฏิกิริยาที่เกิดขึ้นคือ
2NO (g) + O2 (g)  2NO2 (g)
2NO2 (g)
2NO (g) + H2O (l) HNO2 (aq) + HNO3 (aq)
HNO2 (aq) + HNO3 (aq)
ความเป็นกรดเบสของน้ำและดินมีความสำคัญต่อการเพาะปลูกและการเลี้ยงสัตว์น้ำ เช่น กุ้ง ซึ่งในการเลี้ยงกุ้ง pH ของน้ำต้องเป็นกลาง กุ้งจึงจะเจริญเติบโตได้ดี เป็นต้น และโดยทั่วไปดินที่มี pH ต่ำ เกินไปอาจจะไม่เหมาะสมต่อการเจริญเติบโตของพืช พืชแต่ละชนิดจะเติบโตในภาวะที่ต่างกัน ข้าวจะเจริญเติบโตในดินเปรี้ยว คือ เป็นกรดเล็กน้อย ดังนั้น จึงต้องมีการตรวจวัด pH ของดินและน้ำ เพื่อช่วยให้เกษตรสามารถจัดการกับการเพาะปลุกได้ดี เช่น ถ้า pH ต่ำมากก็อาจใช้ปูนขาว หรือขึ้เถ้าโรยลงไปในดินเพื่อลดความเป็นกรดของดินได้2NO (g) + H2O (l)
ปฏิกิริยาระหว่างกรดกับเบส,ปฏิกิริยาของกรดหรือเบสกับสารบางชนิด,
เกลือ,ประโยชน์ของเกลือ,ปฏิกิริยาไฮโดรไลซีสของเกลือ
1.ปฏิกิริยาระหว่างกรดกับเบส
จากทฤษฎีกรด-เบสของเบรินสเตตและลาวรี กรดคือสารที่ให้โปรตอน และเบสคือ สารที่รับโปรตอน เมื่อกรดทำปฏิกิริยากับเบส จึงมีการถ่ายโอนโปรตอนระหว่างกรดและเบสนั่นเอง ตัวอย่างเช่น ปฏิกิริยาระหว่าง HCl และ NaOH สามารถเขียนปฏิกิริยาได้ดังนี้
HCl (aq) + NaOH (aq) HCl เป็นกรดจะให้โปรตอน (H+) กับเบส NaOH ได้เกลือ NaCl กับน้ำ โปรตอนถ่ายโอนจากกรด HCl ไปให้กับเบส NaOH เมื่อเขียนสมการไอออนิกสุทธิระหว่างกรดและเบสจะได้ดังนี้
H+ (aq) + OH- (aq)
ปฏิกิริยาระหว่าง H+ จากสารละลายกรดกับ OH- จากสารละลายเบสได้ H2O เรียกว่า ปฏิกิริยาสะเทิน (Neutralization reaction) ปฏิกิริยาระหว่างกรดกับเบส จะได้เกลือกับน้ำเป็นส่วนใหญ่ แต่จะมีบางปฏิกิริยาที่ได้เกลือเพียงอย่างเดียว เช่น ปฏิกิริยาระหว่าง HCl กับ NH3 ได้เกลือ NH4Cl ซึ่งเกลือ NH4Cl จะแตกตัวให้ NH4+ และ Cl- ทำให้สารละลายนำไฟฟ้าได้
HCl (aq) + NH3
NH4Cl (aq)
ตัวอย่างปฏิกิริยาระหว่างกรดซัลฟิวริกกับแบเรียมไฮดรอกไซด์จะได้ตะกอน BaSO4 กับน้ำ
H2SO4 (aq) + Ba(OH)2 (aq)
สารละลาย H2SO4 และสารละลาย BaSO4 นำไฟฟ้าได้ แต่เมื่อนำมาผสมเข้าด้วยกันแล้วสารละลายที่ได้ไม่สามารถนำไฟฟ้าได้เพราะ BaSO4 เป็นของแข็งที่ละลายน้ำได้น้อยมาก จึงมีไอออนที่จะนำไฟฟ้าได้อยู่น้อยมาก ซึ่งไอออนที่เกิดขึ้นอาจเกิดขึ้นเนื่องจากการแตกตัวของน้ำ ทำให้สารละลายผสมสามารถนำไฟฟ้าได้เล็กน้อย
ปฏิกิริยาระหว่างกรดกับเบส สามารถแบ่งได้ดังนี้
1.ปฏิกิริยาระหว่างกรดแก่กับเบสแก่
เช่น ปฏิกิริยาระหว่างกรดแก่ HCl กับเบสแก่ KOH ได้เกลือ KCl และน้ำ ดังนี้HCl (aq) + KOH (aq)
2.ปฏิกิริยาระหว่างกรดแก่กับเบสอ่อน
เช่น ปฏิกิริยาระหว่างกรดแก่ HCl กับเบสอ่อน NH4OH ได้เกลือ NH4Cl และน้ำHCl (aq) + NH4OH (aq)
3.ปฏิกิริยาระหว่างกรดอ่อนกับเบสแก่
เช่น ปฏิกิริยาระหว่างกรด CH3COOH และเบส NaOH ได้เกลือโซเดียมแอซิเตต (CH3COONa) และน้ำCH3COOH (aq) + NaOH (aq)
4.ปฏิกิริยาระหว่างกรดอ่อนกับเบสอ่อน
เช่น ปฏิกิริยาระหว่างกรด HCN กับเบส NH4OH ได้เกลือ NH4CN และน้ำHCN (aq) + NH4OH (aq)
ปฏิกิริยาระหว่างกรดและเบสในน้ำนี้จะทำให้สารละลายที่ได้แสดงสมบัติเป็นกรด เบส หรือกลางได้ ซึ่งพิจารณาได้เป็น 2 กรณี
1.ในกรณีกรดและเบสทำปฏิกิริยากันแล้วมีกรดหรือเบสเหลืออยู่ ถ้ามีกรดเหลืออยู่สารละลายแสดงสมบัติเป็นกรด ถ้ามีเบสเหลืออยู่สารละลายก็จะแสดงสมบัติเป็นเบส
2.ถ้ากรดกับเบสทำปฏิกิริยากันหมดพอดี ได้เกลือกับน้ำ สารละลายของเกลือที่ได้จากปฏิกิริยา จะแสดงสมบัติเป็นกรด เบส หรือกลาง ขึ้นอยู่กับชนิดของเกลือนั้นว่ามาจากกรดและเบสประเภทใด ทั้งนี้เพราะเกลือแต่ละชนิดจะเกิดการแตกตัวและทำปฏิกิริยากับน้ำ เรียกว่า ไฮโดรไลซีส ซึ่งจะทำให้สารละลายแสดงสมบัติกรด-เบสต่างกัน รายละเอียดอยู่ในหัวข้อต่อไป
2.ปฏิกิริยาของกรดหรือเบสกับสารบางชนิด
กรดนอกจากจะสามารถทำปฏิกิริยาสะเทินกับเบสได้เกลือกับน้ำ แล้วยังสามารถทำปฏิกิริยากับโลหะบางชนิด เช่น Zn, Fe, ได้แก๊ส H2 และเกลือของโลหะนั้น หรือทำปฏิกิริยากับเกลือคาร์บอนเนต เช่น CaCO3 , Na2CO3 หรือเกลือ NaHCO3 ได้แก๊ส CO2ตัวอย่างปฏิกิริยาระหว่าง HCl กับ CaCO3 จะได้เกลือและแก๊ส CO2
HCl(aq) + CaCO3 (s)
เบสก็เช่นเดียวกันนอกจากจะทำปฏิกิริยาสะเทินกับกรดได้เกลือกับน้ำแล้ว ยังสามารถทำปฏิกิริยากับเกลือแอมโมเนียมเช่น NH4Cl, (NH4)2SO4 , จะได้แก๊ส NH3 หรือทำปฏิกิริยากับเกลือ เช่นปฏิกิริยาระหว่าง NaOH กับ FeCl3 ได้สารผลิตภัณฑ์ดังนี้
3NaOH (aq) + FeCl3 (aq)
ดังนั้น จะเห็นได้ว่ากรดและเบสทำปฏิกิริยากันเองได้ และทั้งกรดและเบสก็สามารถทำปฏิกิริยากับสารอื่นได้ด้วย
เกลือ (Salt)
เกลือเป็นสารประกอบไอออนิก ประกอบด้วยไอออนบวก (แคตไอออน) และไอออนลบ (แอนไอออน) ยกเว้น OH- ตัวอย่างเช่น NaCl ประกอบด้วยโซเดียมไอออน (Na+) และคลอไรด์ไอออน (Cl-) แบเรียมซัลเฟต (BaSO4) ประกอบด้วยแบเรียมไอออน (Ba2+) และซัลเฟตไอออน (SO42-) เกลือ NaCl ละลายในน้ำได้ดีและให้ Na+ และ Cl- แต่เกลือ BaSO4 เป็นเกลือที่ไม่ละลายน้ำ ทำให้สารละลายของเกลือ NaCl นำไฟฟ้าได้ดี แต่สารละลายของเกลือ BaSO4 ไม่นำไฟฟ้าเราอาจจำแนกเกลือออกได้เป็นประเภทต่างๆ ดังนี้
1.เกลือปกติ (Normal salt)
เกลือปกติเป็นเกลือที่ไม่มีไฮโดรเจนหรือไฮดรอกไซด์ไอออนที่อาจถูกแทนที่ ดังนั้น จึงประกอบด้วยไอออนบวกคือโลหะ หรือกลุ่มธาตุที่เทียบเท่าโลหะ เช่น NH4+ (แอมโมเนียมไอออน) กับไอออนลบซึ่งเป็นอนุมูลกรด (Acid radical) ตัวอย่างของเกลือปกติ เช่น NaCl, K2SO4 , Ca3(PO4)2 , NH4NO3 , (NH4)2SO4 , ZnSO4 เป็นต้น2.เกลือกรด (Acid salt)
เกลือประเภทนี้มี H อะตอมอยู่ในโมเลกุลของเกลือ ซึ่งสามารถไอออไนซ์ได้ (แตกตัวเป็นไอออนได้) เช่น NaHSO4 , NaHCO3 , Na2HPO4 , NaH2PO4 เป็นต้น3.เกลือเบสิก (Base salt)
เกลือประเภทนี้มีไอออนลบ OH- และไอออนบวก เช่น Pb(OH)Cl, Bi(OH)2Cl เป็นต้น4.เกลือสองเชิง (Double salt)
เกิดจากเกลือปกติสองชนิดรวมกันเป็นโมเลกุลใหญ่ เช่น K2SO4 , Al(SO4)3.24H2O เป็นต้น5.เกลือเชิงซ้อน (Complex salt)
ประกอบด้วยไอออนลบที่ไอออนเชิงซ้อน เช่น K3Fe(CN)6 เป็นต้นการเรียกชื่อเกลือ
1.ให้อ่านโลหะแล้วตามด้วยอนุมูลกรด เช่นNaCl = โซเดียมคลอไรด์
KI = โพแทสเซียมไอโอไดด์
MgS = แมกนีเซียมซัลไฟด์
ถ้าอนุมูลกรดมาจากกรดที่ลงท้ายด้วย ous ต้องเปลี่ยนเป็น ite แต่ถ้าลงท้ายด้วย ic ต้องเปลี่ยนเป็น ate เช่น
Na2CO3 = โซเดียมคาร์บอเนต
Ca3(PO4)2 = แคลเซียมฟอสเฟต
K2SO4 = โพแทสเซียมซัลเฟต
Na2SO4 = โซเดียมซัลเฟต
2.ถ้าโลหะมีเลขออกซิเดชัน (ประจุไฟฟ้า) มากกว่า 1 ค่าให้บอกไว้ในวงเล็บหลังโลหะนั้น แล้วอ่านตามด้วยอนุมูลกรด เช่น
Fe(NO3)2 = ไอร์ออน (II) ไนเตรต
Fe(NO3)3 = ไอร์ออน (III) ไนเตรต
SnCl2 = ทิน (II) คลอไรด์
SnCl4 = ทิน (IV) คลอไรด์
วิธีการเตรียมเกลือ
1.เตรียมจากปฏิกิริยาระหว่างกรดกับเบส
กรด + เบสเช่น HCl (aq) + NaOH (aq)
H2SO4 (aq) + Ba(OH)2 (aq)
“เกลือที่เกิดจากกรดและเบสทำปฏิกิริยากัน ไอออนบวกของเกลือจะมาจากเบส ส่วนไอออนลบของเกลือมาจากกรด”
เกลือที่เกิดจากปฏิกิริยาระหว่างกรดกับเบส แบ่งออกได้เป็น
1.1 เกลือที่เกิดจากกรดแก่และเบสแก่ ตัวอย่างเช่น- NaCl เกิดจากกรด HCl กับเบส NaOH,
HCl (aq) + NaOH (aq)
- Ca(NO3)2 เกิดจาก HNO3 และ Ca(OH)2
HNO3 (aq) + Ca(OH)2 (aq)
1.2 เกลือที่เกิดจากกรดอ่อนกับเบสแก่ เช่น
- NaClO เกิดจาก HClO และ NaOH
HClO (aq) + NaOH (aq)
- Ba(C2H3O2)2 เกิดจาก C2H3O2H และ Ba(OH)2
C2H3O2H(aq) + Ba(OH)2(aq)
1.3 เกลือที่เกิดจากกรดแก่กับเบสอ่อน เช่น
- NH4Cl เกิดจาก HCl กับ NH3
HCl (aq) + NH3 (g)
- Al(NO3)3 เกิดจาก HNO3 (aq) และ Al(OH)3 (aq)
HNO3 (aq) + Al(OH)3 (aq)
1.4 เกลือที่เกิดจากกรดอ่อนและเบสอ่อน เช่น
- NH4CN เกิดจากกรด HCN กับเบส NH3
HCN(aq) + NH3 (g)
- FeCO3 เกิดจากกรด H2CO3 (aq) กับเบส Fe(OH)2 (aq)
H2CO3 (aq) + Fe(OH)2 (aq)
2. เตรียมจากปฏิกิริยาของโลหะกับกรด
โลหะ + กรดโลหะ + กรด
เช่น
Mg (s) + 2HCl (aq)
Zn(s) + H2SO4 (aq)
3Cu(s) + 8HNO3 (aq)
3. เตรียมจากปฏิกิริยาของโลหะออกไซด์กับกรด
โลหะออกไซด์ + กรดเช่น CaO (s) + H2SO4 (aq)
CuO (s) + H2SO4 (aq)
MgO (s) + 2HCl (aq)
4. เตรียมจากปฏิกิริยาของเกลือกับกรด เช่น
FeS(s) + 2HCl (aq)
Na2CO3 (s) + H2SO4 (aq)
NaHCO3 (s) + HCl(aq)
BaCO3 (s) + 2HCl (aq)
5.เตรียมจากปฏิกิริยาของเกลือกับเกลือ
NaCl (aq) + AgNO3 (aq)BaCl2 (aq) + Na2SO4 (aq)
ZnCl2 (aq) + Na2S (aq)
6.โดยการรวมตัวกันโดยตรงของโลหะกับอโลหะ
2Na(s) + Cl2 (g)Fe (s) + S (s)
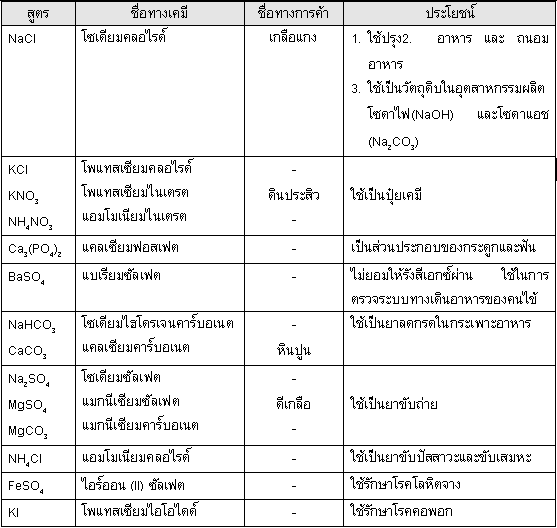
เกลือหลายชนิดมีประโยชน์มากทั้งในชีวิตประจำวัน และในอุตสาหกรรม ดังแสดงในตาราง
ตัวอย่างที่ 1 จงเขียนสมการ และเรียกชื่อเกลือที่เกิดจากปฏิกิริยาระหว่างสาร ต่อไปนี้
ก. กรดคาร์บอนิก กับแคลเซียมไฮดรอกไซด์
ข. โซเดียมซัลไฟด์กับกรดซัลฟิวริก
ค. เหล็กกับกรดไฮโดรคลอริก
วิธีทำ
ก. H2CO3 (aq) + Ca(OH)2 (aq)
แคลเซียมคาร์บอเนต
ข. Na2S (s) + H2SO4 (aq)
โซเดียมซัลเฟต
หรืออาจเกิดปฏิกิริยาได้อีกแบบหนึ่งดังนี้
Na2S (s) + 2H2SO4 (aq)
โซเดียมไฮโดรเจนซัลเฟต
ค. Fe(s) + 2HCl(aq)
ไอร์ออน(II) คลอไรด์
ตัวอย่างที่ 2 จะต้องใช้สาระลายกรดและเบสคู่ใดทำปฏิกิริยากันจึงจะได้เกลือต่อไปนี้
ก. KBr
ข. NH4NO3
ค. BaSO4
ง. NH4HCO3
วิธีทำ
ก. KOH (aq) + HBr (aq)
ข. NH4OH (aq) + HNO3 (aq)
ค. H2SO4 (aq) + Ba(OH)2 (aq)
ง. H2CO3 (aq) + NH4OH (aq)
ตัวอย่างที่ 3 จงเขียนสมการแสดงปฏิกิริยา ระหว่างสารต่อไปนี้พร้อมทั้งเรียกชื่อเกลือที่เกิดขึ้นด้วย
ก. CH3COOH กับ Ca(OH)2
ข. HCl กับ Na2CO3
ค. H2SO4 กับ NaOH
วิธีทำ
ก. CH3COOH (aq) + Ca(OH)2 (aq)
แคลเซียมแอซิเตต
ข. 2HCl (aq) + Na2CO3 (s)
โซเดียมคลอไรด์
ค. H2SO4 (aq) + NaOH (aq)
โซเดียมไฮโดรเจนซัลเฟต
หรือ
H2SO4 (aq) + 2NaOH (aq)
โซเดียมซัลเฟต
3.ปฏิกิริยาไฮโดรไลซีสของเกลือ (Hydrolysis of Salts)
ไฮโดรไลซีส หมายถึง ปฏิกิริยาระหว่างสาร(เกลือ) กับน้ำไฮโดรไลซีสของเกลือ หมายถึง ปฏิกิริยาระหว่างเกลือกับน้ำ เกลือเป็นอิเล็กโทรไลต์แก่ เมื่อเกลือละลายในน้ำ เกลือจะแตกตัวออกเป็นไอออนบวกและไอออนลบทั้งหมด ดังนั้น สมบัติของสารละลายของเกลือ จึงขึ้นอยู่กับไอออนบวกและไอออนลบในสารละลายนั้น ไอออนบางตัวสามารถที่จะทำปฏิกิริยากับน้ำและให้ H+ หรือ OH- ได้ ปฏิกิริยานี้จึงเรียกว่า ปฏิกิริยาไฮโดรไลซีส เช่น
- ไอออนลบ เช่น X- เมื่อทำปฏิกิริยากับน้ำ จะเขียนสมการได้ดังนี้
X- (aq) + H2O (l)
จะเห็นว่าจากปฏิกิริยาไฮโดรไลซีสของไอออนลบ X- ที่เกิดขึ้น X- (aq) จะรับ H+ จากน้ำแล้วได้ OH- (aq) ดังนั้นสารละลายที่ได้จึงมีสมบัติเป็นเบส
- สำหรับไอออนบวก เช่น NH4+(aq) เมื่อทำปฏิกิริยากับน้ำ จะเขียนสมการได้ดังนี้
NH4+ (aq) + H2O(l)
จะเห็นว่าจากปฏิกิริยาไฮโดรไลซีสของไอออนบวก NH4+(aq) ที่เกิดขึ้น NH4+ จะให้โปรตอนกับ H2O (l) แล้วได้ H3O+ (aq) ดังนั้นสารละลายที่ได้จึงมีสมบัติเป็นกรด
ดังนั้นจึงอาจสรุปได้ว่า “ถ้าไอออนลบของเกลือเกิดปฏิกิริยาไฮโดรไลซีสจะทำให้สารละลายแสดงสมบัติความเป็นเบส และถ้าไอออนบวกของเกลือเกิดปฏิกิริยาไฮโดรไลซีส จะทำให้สารละลายแสดงสมบัติความเป็นกรด”
- การพิจารณาว่าไอออนลบใดจะเกิดไฮโดรไลซีสหรือไม่นั้นมีหลักพิจารณาดังนี้
1. ถ้าเป็นไอออนลบของกรดแก่ เช่น Cl-, Br- , I- , NO3- , และ ClO4- จะไม่ทำปฏิกิริยากับน้ำ ดังนั้น จะไม่มีผลต่อค่าความเป็นกรด-เบสของสารละลาย
2. ไอออนลบของกรดอ่อน เช่น CH3COO- , ClO- , CN- , และ CO32- สามารถรับโปรตอนจากน้ำเกิดปฏิกิริยาไฮโดรไลซีสได้สารละลายที่เป็นเบส เช่น ปฏิกิริยาของ CH3COO- กับน้ำ
CH3COO- (aq) + H2O (l)
- การพิจารณาว่าไอออนบวกใดจะเกิดปฏิกิริยาไฮโดรไลซีสหรือไม่มีหลักพิจารณาดังนี้
1. ไอออนบวกของโลหะหมู่ IA หรือ IIA (ยกเว้น Be) ได้แก่ Li+ , Na+ , K+ , Mg2+ , Ca2+ และ Ba2+ จะไม่เกิดปฏิกิริยาไฮโดรไลซีส รวมทั้งไอออนบวกของเบสแก่ทั้งหมด
2. แอมโมเนียมไอออนของเกลือแอมโมเนียมจะเกิดปฏิกิริยาไฮโดรไลซีส และทำให้สารละลายเป็นกรด
1. การไฮโดรไลซีสของเกลือที่เกิดจากกรดแก่และเบสแก่
เกลือประเภทนี้เมื่อละลายในน้ำจะไม่เกิดปฏิกิริยาไฮโดรไลซีสกับน้ำ ทั้งนี้เพราะ ทั้งไอออนบวกที่มาจากเบสแก่ และไอออนลบที่มจากกรดแก่ ต่างก็ไม่ทำปฏิกิริยากับน้ำ เช่น NaCl เมื่อละลายน้ำได้ Na+ และ Cl- ทั้ง Na+ ซึ่งมาจากเบสแก่ และ Cl- ซึ่งมาจากกรดแก่ HCl จะไม่ทำปฏิกิริยากับน้ำ ไม่มีผลต่อค่า pH ของสารละลาย สารละลายจึงเป็นกลาง คือมี [H3O+] และ [OH-] ที่แตกตัวจากน้ำมีปริมาณเท่ากัน pH ของสารละลายเท่ากับ 72. การไฮโดรไลซีสของเกลือที่เกิดจากกรดอ่อนกับเบสแก่
เกลือประเภทนี้เมื่อละลายน้ำจะได้ไอออนลบที่มาจากกรดอ่อนที่มีสมบัติเป็นคู่เบสที่แรงพอสมควร ไอออนลบที่เกิดขึ้นจะเกิดปฏิกิริยาไฮโดรไลซีสกับน้ำได้ OH- ไอออนทำให้สารละลายแสดงสมบัติความเป็นเบสตัวอย่างเช่น NaClO เมื่อละลายน้ำจะให้ Na+ และ ClO- ดังนี้
NaClO (s)
ClO- จะเกิดปฏิกิริยาไฮโดรไลซีส โดยรับโปรตอนจากน้ำได้เป็น HClO และ OH- ตามสมการ
ClO- (aq) + H2O (l)
สำหรับ Na+ (aq) ไอออน ซึ่งมาจากเบสแก่ NaOH ไม่เกิดการไฮโดรไลซีส
ดังนั้นสารละลายที่เกิดจากการละลายของเกลือ NaClO ในน้ำแล้วเกิดการไฮโดรไลซีสของ ClO- (aq) จะได้ OH- ไอออน จึงแสดงสมบัติเป็นเบส pH ของสารละลายมีค่ามากกว่า 7
3. การไฮโดรไลซีสของเกลือที่เกิดจากกรดแก่กับเบสอ่อน
เกลือประเภทนี้เมื่อละลายน้ำจะให้ไอออนบวกที่มาจากเบสที่เป็นคู่กรด ที่มีความแรงพอสมควร ไอออนบวกนี้จะเกิดปฏิกิริยาไฮโดรไลซีสกับน้ำให้ H3O+ ทำให้สารละลายแสดงสมบัติเป็นกรดส่วนไอออนลบซึ่งมาจากกรดแก่ ไม่เกิดปฏิกิริยาไฮโดรไลซีส ตัวอย่างเช่น
NH4Cl ซึ่งเกิดจากกรดแก่ HCl กับเบสอ่อน NH3
NH4Cl แตกตัวในน้ำได้ NH4+ และ Cl- ทั้งหมด
NH4Cl (aq)
Cl- ไม่เกิดการไฮโดรไลซีส แต่ NH4+ เกิดไฮโดรไลซีส โดย NH4+ จะให้โปรตอนกับ H2O ได้เป็น NH3(aq) และ H3O (aq) ดังสมการ
NH4+ (aq) + H2O (l)
จะเห็นได้ว่าผลจากการไฮโดรไลซีสของ NH4Cl จะได้ H3O+ ดังนั้นสารละลายของเกลือ NH4Cl จึงแสดงสมบัติเป็นกรด pH ของสารละลายมีค่าน้อยกว่า 7
4.การไฮโดรไลซีสของเกลือที่เกิดจากกรดอ่อนและเบสอ่อน
เกลือประเภทนี้เมื่อละลายน้ำได้ไอออนบวกและไอออนลบ ซึ่งไอออนทั้งสองนี้ สามารถเกิดปฏิกิริยาไฮโดรไลซีสได้ทั้งคู่ ไอออนบวกของเกลือจะเกิดปฏิกิริยาไฮโดรไลซีสได้ H3O+ ส่วนไอออนลบได้ OH- ดังนั้นความเป็นกรด-เบสของสารละลายจึงขึ้นอยู่กับว่าไอออนบวกหรือไอออนลบเกิดปฏิกิริยาการไฮโดรไลซีสได้ดีกว่ากัน โดยพิจารณาจากค่าคงที่ของการแตกตัวของคู่เบส (Kb) (ไอออนลบ) หรือค่าคงที่การแตกตัวของคู่กรด Ka (ไอออนบวก)ตัวอย่างเช่น เกลือ NH4CN ที่เกิดจากกรดอ่อน HCN และเบสอ่อน NH4OH
NH4OH แตกตัวในน้ำให้ NH4+ และ CN- ดังสมการ
NH4CN (aq)
NH4+ และ CN- เกิดปฏิกิริยาการไฮโดรไลซีสดังนี้
NH4+ (aq) + H2O (l)
CN- (aq) + H2O (l)
เนื่องจาก ค่า Kb> Ka ดังนั้นแสดงว่า CN- เกิดปฏิกิริยาไฮโดรไลซีสให้ OH- ได้ดีกว่า NH4+ ดังนั้น [OH-] > [NH3] สารละลายของเกลือ NH4CN จึงแสดงสมบัติเป็นเบส pH มีค่ามากกว่า 7
ตัวอย่างที่ 4 จงเขียนสมการแสดงการละลายน้ำของเกลือโซเดียมแอซิเตต และให้บอกว่าสารละลายเป็นกรดหรือเบส
วิธีทำ
เกลือโซเดียมแอซิเตต มีสูตรโมเลกุลเป็น CH3COONa เมื่อละลายน้ำจะแตกตัวให้ Na+ และ CH3COO- หมดดังสมการ
CH3COONa (s)
Na+ ไอออน ไม่เกิดปฏิกิริยาไฮโดรไลซีส
CH3COO- เกิดปฏิกิริยาไฮโดรไลซีส โดย CH3COO- รับโปรตอนจากน้ำได้เป็นกรดแอซิติก
CH3COO- (aq) + H2O (l)
จะเห็นว่าผลจากการเกิดปฏิกิริยาไฮโดรไลซีสได้ OH- ดังนั้นสารละลายของเกลือโซเดียมแอซิเตตจึงมีสมบัติเป็นเบส
ตัวอย่างที่ 5 F- ไอออนเกิดปฏิกิริยาการไฮโดรไลซีสหรือไม่ ถ้าเกิดสารละลายเป็นกรดหรือเบส
วิธีทำ F- ไอออนเป็นไอออนลบของเกลือที่เกิดจากกรดอ่อน HF ดังนั้น F- ไอออนเป็นคู่เบสที่มีความแรงเมื่อทำปฏิกิริยากับน้ำจึงสามารถรับโปรตอนจากน้ำได้เป็น HF และ OH- ดังสมการ
F- (aq) + H2O (l)
จะเห็นได้ว่าผลจากการเกิดปฏิกิริยาไฮโดรไลซีสของ F- จะได้ OH- ดังนั้นสารละลายจึงแสดงสมบัติความเป็นเบส
ตัวอย่างที่ 6 NH4Br เมื่อละลายน้ำจะมีผลต่อค่า pH ของสารละลายอย่างไร ?
วิธีทำ NH4Br ละลายในน้ำจะแตกตัวให้NH4+ และ Br-
NH4Br (s)
Br- มาจากกรดแก่ HBr จึงไม่เกิดปฏิกิริยาไฮโดรไลซีส
NH4+ เกิดปฏิกิริยาไฮโดรไลซีสได้ H3O+ ทำให้สารละลายแสดงสมบัติความเป็นกรดโดย ให้ H+ กับน้ำได้ NH3 (aq) และ H3O+ (aq) ดังนี้
NH4+ (aq) + H2O (l)
5.การไฮโดรไลซีสของไอออนลบของเกลือที่เกิดจากกรดพอลิโปรติก
ไอออนลบของเกลือที่เกิดจากกรดพอลิโปรติก เช่น CO32- , PO43- สามารถเกิดปฏิกิริยาการไฮโดรไลซีสได้หลายขั้น เนื่องจากสามารถรับ H+ จาก H2O ได้มากกว่า 1 โปรตอน เช่นปฏิกิริยาการไฮโดรไลซีสของเกลือ Na2CO3 (s)
เมื่อ เกลือ Na2CO3 (s) ละลายน้ำ จะเกิดการแตกตัวเป็นไอออนได้หมด คือ
Na2CO3 (s)
Na+ ไม่เกิดปฏิกิริยาไฮโดรไลซีส เนื่องจากมาจาก เบสแก่ NaOH
CO32- (aq) เกิดปฏิกิริยาการไฮโดรไลซีสได้ 2 ขั้นตอนดังนี้
CO32- (aq) + H2O (l) HCO3- (aq) + OH- (aq)
HCO3- (aq) + OH- (aq)
และ HCO3- (aq) + H2O (l) H2CO3 (aq) + OH- (aq)
H2CO3 (aq) + OH- (aq)
และ HCO3- (aq) + H2O (l)
การไทเทรตกรด-เบส,อินดิเคเตอร์กับการไทเทรตกรด-เบส,การทดลองไทเทรต
การไทเทรตกรด-เบส (Acid-base titration)
การไทเทรตกรด-เบส หมายถึง กระบวนการหาปริมาณสาร โดยวิธีใช้สารละลายมาตรฐานที่ทราบค่าความเข้มข้นที่
แน่นอน ให้ทำปฏิกิริยากับสารตัวอย่าง โดยอาศัยหลักการเกิดปฏิกิริยาระหว่างสารละลายกรดและเบสที่เข้าทำปฏิกิริยา กันพอดี ทำให้คำนวณหาความเข้มข้นหรือปริมาณของสารตัวอย่างดังกล่าวได้
วิธีการไทเทรตกรด-เบส คือ นำสารละลายกรดหรือเบสตัวอย่างที่ต้องการวิเคราะห์หาปริมาณ มาทำการไทเทรตกับสารละลายเบสหรือกรดมาตรฐานที่ทราบค่าความเข้มข้นที่แน่นอน กล่าวคือ ถ้าสารละลายตัวอย่างเป็นสารละลายกรด ก็ต้องใช้สารละลายมาตรฐานเป็นเบส นำมาทำการไทเทรต แล้วบันทึกปริมาตรของสารละลายมาตรฐานที่ใช้ในการทำปฏิกิริยาพอดีกัน จากนั้นนำไปคำนวณหาปริมาณของสารตัวอย่างต่อไป หรือทางตรงกันข้าม ถ้าใช้สารละลายตัวอย่างเป็นเบส ก็ต้องใช้สารละลายมาตรฐานเป็นกรด
ตัวอย่างเช่น การหาค่าสารละลายกรด HCl ว่ามีความเข้มข้นเท่าใดเราอาจใช้สารละลายมาตรฐาน NaOH เข้มข้น 0.100 โมล/ลิตร มาทำการไทเทรตกับสารละลาย HCl ตัวอย่าง จำนวนหนึ่ง (อาจจะเป็น 50 cm3 ) เมื่อทราบปริมาตรของ NaOH ที่ใช้ในการทำปฏิกิริยาพอดีกับ HCl จำนวน 50 cm3 นี้โดยอินดิเคเตอร์เป็นตัวบอกจุดยุติ แล้วเราก็สามารถคำนวณหาความเข้มข้นของกรด HCl ได้
สารละลายมาตรฐาน ที่ทราบความเข้มข้นแน่นอน บรรจุอยู่ในเครื่องแก้วที่เรียกว่า บิวเรตต์ ซึ่งจะมีก๊อกไขปิด-เปิดเพื่อหยดสารละลายมาตรฐานมายังขวดรูปกรวยที่บรรจุสาร ละลายตัวอย่างที่ต้องการวิเคราะห์ ในการไทเทรต ค่อยๆ หยดสารละลายมาตรฐานลงมาทำปฏิกิริยากับสารตัวอย่างในขวดรูปกรวย เขย่าหรือหมุนขวดรูปกรวยเพื่อให้สารผสมกันพอดี ไทเรตจนกระทั่งอินดิเคเตอร์เปลี่ยนสีก็หยุดไทเทรต แล้วบันทึกปริมาตรสารละลายมาตรฐานที่ใช้ เพื่อนำไปคำนวณหา pH สารละลายต่อไป
เครื่องแก้วเชิงปริมาตร ที่ใช้ในการถ่ายเทของเหลวตัวอย่าง ลงในขวดรูปกรวยจะใช้เครื่องแก้วที่สามารถ อ่านปริมาตรได้ค่าที่ละเอียด และมีค่าถูกต้องมากที่สุด นั่นคือจะใช้ ปิเปตต์ (จะไม่ใช้กระบอกตวงเพราะให้ค่าที่ไม่ละเอียด และความถูกต้องน้อย) ซึ่งมีขนาดต่างๆ ให้เลือกใช้ เช่น ขนาด 1 cm3 , 5, 10, 25, 50 cm3 เป็นต้น วิธีใช้ปิเปตต์จะใช้ลูกยางช่วยในการดูดสารละลาย โดยในตอนแรก บีบอากาศออกจากลูกยาง ที่อยู่ปลายบนของปิเปตต์ แล้วจุ่มปลายปิเปตต์ ลงในสารละลายที่ต้องการปิเปตต์ แล้วค่อยๆ ปล่อยลูกยาง สารละลายจะถูกดูดขึ้นมาในปิเปตต์ เมื่อสารละลายอยู่เหนือขีดบอกปริมาตร ดึงลูกยางออก รีบใช้นิ้วชี้กดที่ปลายปิเปตต์ค่อยๆ ปล่อยสารละลายออกจนถึงขีดบอกปริมาตรบน จากนั้นก็ปล่อยสารละลาย ออกจากปิเปตต์สู่ขวดรูปกรวยจนหมด

การไทเทรตกรด-เบส

รูปแสดงการใช้ปิเปตต์

รูปแสดงการใช้บิวเรตต์
อินดิเคเตอร์กับการไทเทรตกรด-เบส
อินดิเคเตอร์กรด-เบส ที่เหมาะสมกับปฏิกิริยาการไทเทรตจะต้องมีค่า pH ที่จุดกึ่งกลางช่วงการเปลี่ยนสีใกล้เคียงหรือเท่ากับ pH ที่จุดสมมูลของปฏิกิริยา นอกจากนี้ การเลือกใช้อินดิเคเตอร์กรด-เบส ต้องพิจารณาสีที่ปรากฎ จะต้องมีความเข้มมากพอที่จะมองเห็นได้ง่าย หรือเห็นการเปลี่ยนสีได้ชัดเจน ช่วงการเปลี่ยนสีของอินดิเคเตอร์ จะเกิดขึ้นในช่วง 2 หน่วย pHตัวอย่างเช่น การไทเทรตกรดแก่กับเบสแก่ pH ของสารละลายผลิตภัณฑ์ที่เกิดจากปฏิกิริยาการไทเทรต เมื่อถึงจุดสมมูลมีค่าใกล้เคียง 7 ก็ควรเลือกใช้อินดิเคเตอร์ที่มีช่วง pH ของการเปลี่ยนสีใกล้เคียงกับ 7 เช่น อาจใช้โบรโมไทมอลบลูหรือ ฟีนอล์ฟทาลีน ซึ่งจะเปลี่ยนจากไม่มีสีเป็นสีชมพู ในช่วง pH 8.20-10.00 เป็นต้น ดังนั้น ถ้าทราบ pH ของสารละลายที่จุดสมมูลของปฏิกิริยาการไทเทรตก็สามารถเลือกอินดิเคเตอร์ที่ เหมาะสมได้
การเลือกอินดิเคเตอร์ ก็ขึ้นอยู่กับชนิดของปฏิกิริยาระหว่างกรดกับเบส เพราะที่จุดสมมูลของแต่ละปฏิกิริยานั้น มีค่า pH ที่ต่างกัน
การฟของการไทเทรตจะช่วยในการเลือกอินดิเคเตอร์ที่เหมาะสมได้ดี เพราะกราฟจะแสดงค่า pH ของสารละลายขณะไทเทรต ตั้งแต่ก่อนจุดสมมูล ที่จุดสมมูล และหลังจุดสมมูล จุดที่ pH ของสารละลายเปลี่ยนแปลงมาก ซึ่งเป็นจุดสมมูลนั้น จะบอกช่วง pH ของอินดิเคเตอร์ที่จะเลือกใช้ ในการพิจารณาเลือกอินดิเคเตอร์ จากกราฟของการไทเทรต จะแบ่งออกตามชนิดของปฏิกิริยาดังนี้
1.อินดิเคเตอร์สำหรับปฏิกิริยาระหว่างกรดแก่กับเบสแก่
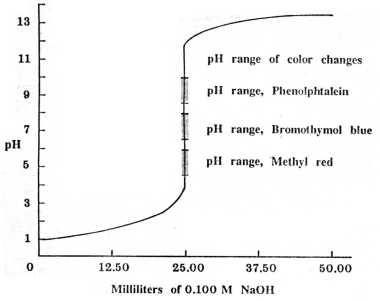
รูปกราฟของการไทเทรตระหว่างกรดแก่และเบสแก่ จะแสดง pH ที่จุดสมมูลอยู่ที่ pH ใกล้เคียง 7
จากกราฟ จะเห็นว่าค่า pH เปลี่ยนแปลงรวดเร็วที่จุดใกล้ๆ จุดยุติ (ตั้งแต่ pH 4-10) ดังนั้นอินดิเคเตอร์ที่มีช่วง pH ของการเปลี่ยนแปลงสีระหว่าง 4 ถึง 10 ก็สามารถนำมาใช้ได้ ซึ่งอินดิเคเตอร์ที่เหมาะสมที่อาจใช้ได้ ได้แก่ เมทิลเรด (4.4-6.2) โบรโมไทมอลบลู (6.0-7.5) และฟีนอล์ฟทาลีน(8.2-10.0) ดังแสดงในภาพ แต่เรามักจะนิยมใช้ฟีนอล์ฟทาลีน เพราะสังเกตการเปลี่ยนแปลงสีได้ชัดเจน สำหรับ โบรโมคลีซอล กรีน (3.8-5.4) ไม่เหมาะสมที่จะใช้เป็นอินดิเคเตอร์สำหรับกรดแก่และเบสแก่ เพราะช่วงเปลี่ยนสีที่เป็นรูปเบสของอินดิเคเตอร์ จะเกิดก่อนจุดสมมูล ทำให้เกิดความคลาดเคลื่อนในการบอกจุดยุติ2.อินดิเคเตอร์สำหรับปฏิกิริยาระหว่างกรดอ่อนกับเบสแก่
การเลือกอินดิเคเตอร์สำหรับการไทเทรตกรดอ่อน เช่น กรดแอซิติก กับเบสแก่ เช่น NaOH จะมีข้อจำกัดมากกว่าที่จุดสมมูลของการไทเทรต สารละลายจะมีโซเดียมแอซิเตต ทำให้สารละลายเป็นเบส มี pH มากกว่า 7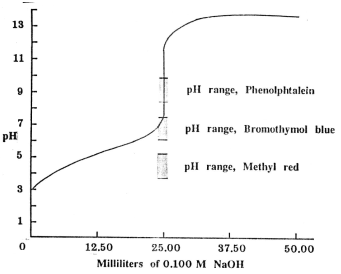
รูปกราฟแสดงการไทเทรตระหว่างกรดอ่อนกับเบสแก่และอินดิเคเตอร์ที่เหมาะสม
จากกราฟจะเห็นได้ว่า เมทิลเรด จะเปลี่ยนสีก่อนจุดสมมูลจึงไม่เหมาะที่จะใช้เป็นอินดิเคเตอร์สำหรับกรดแอซิติกกับ NaOH (เข้มข้น 0.100 M) ฟีนอล์ฟทาลีนเปลี่ยนสีที่ช่วงจุดสมมูลพอดี โบรโมไทมอลบลู อาจจะใช้เป็นอินดิเคเตอร์ได้ดี เมื่อใช้สีมาตรฐานเทียบ3.อินดิเคเตอร์สำหรับปฏิกิริยาระหว่างกรดแก่กับเบสอ่อน
การเปลี่ยนแปลง pH ของสารละลายขณะไทเทรตเบสอ่อน เช่น NH3 กับกรดแก่ เช่น HCl จะค่อยๆ ลดลง เมื่อใช้ HCl เป็นสารมาตรฐาน ที่จุดยุติจะได้เกลือ NH4Cl และ pH < 7 ในการไทเทรต 0.100 M NH3 กับ 0.100 M HCl จะได้กราฟของการไทเทรต (ดังภาพ)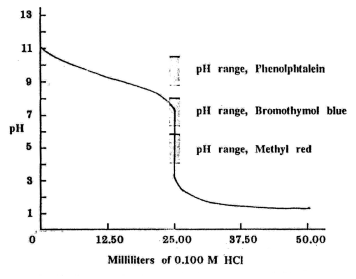
จากกราฟ เราสามารถพิจารณาชาวง pH 3-7.5 ในการเลือกอินดิเคเตอร์ ซึ่งเราอาจใช้โบรโมไทมอลบลูหรือเมทิลเรดได้ แต่ไม่ควรใช้ฟีนอล์ฟทาลีนเพราะช่วง pH ของฟีนอล์ฟทาลีนมากกว่า 7 ทำให้เกิดความคลาดเคลื่อนในการบอกจุดสมมูล
ตัวอย่างที่ 1 กำหนดช่วง pH ของอินดิเคเตอร์ให้ดังนี้
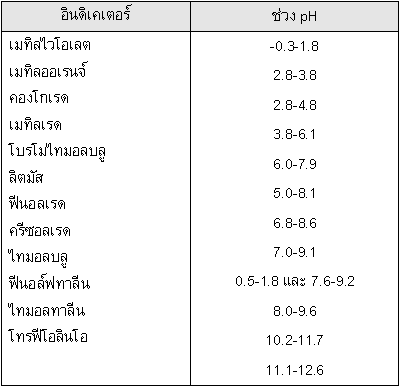
วิธีทำ
HCN (aq) + NaOH(aq)
| เพราะฉะนั้นจำนวนโมลของ HCN = | = 5 x 10-3 โมล | |
| เพราะฉะนั้นจำนวนโมลของ NaOH = | = 5 x 10-3 โมล | |
| เพราะฉะนั้น [NaCN] = | x 5 x 10-3 = 0.05 โมล/ลิตร |
NaCN (aq)
0.05 0.05 0.05 โมล/ลิตร
CN- (aq) + H2O
ความเข้มข้นเริ่มต้น 0.05 0 0
ความเข้มข้นที่เปลี่ยนไป -x +x +x
ความเข้มข้นที่ภาวะสมดุล 0.05-x x x

| 1.4 x 10-5 = | ||
| 1.4 x 10-5 = | ( | |
pOH = -log[OH-] = -log[8.4 x 10-4] = -0.92 + 4 = 3.08
pH = 14 - pOH = 14 - 3.08 = 10.92
เนื่องจาก pH ของสารละลายหลังไทเทรตเท่ากับ 10.92 ดังนั้นจะต้องเลือกใช้อินดิเคเตอร์ไทมอลทาลีน ซึ่งมีช่วงการเปลี่ยนแปลง pH อยู่ระหว่าง 10.2-11.7 จึงจะเหมาะสมที่สุด
ตัวอย่างที่ 2 นำสารละลาย HA ซึ่งเป็นกรดอ่อนชนิดหนึ่งปริมาตร 50.00 cm3 ไปไทเทรตกับสารละลายมาตรฐาน NaOH เข้มข้น 0.15 โมล/ลิตร พบว่าเมื่อเติม NaOH ลงไป 12.00 cm3 จะทำให้สารละลายที่ได้มี pH 7 และเมื่อเติม NaOH ลงไป 16.00 cm3 จะถึงจุดยุติพอดี สารละลายกรด HA มีความเข้มข้นเริ่มต้นเท่าใด และการไทเทรตกรด-เบสคู่นี้ควรใช้อินดิเคเตอร์ชนิดใด (กำหนด Ka ของกรดอ่อน HA = 1.7 x 10-6) กำหนดให้
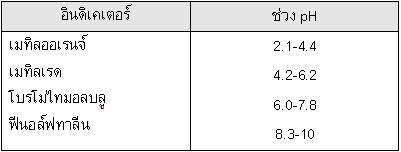
ที่จุดยุติจำนวนโมล NaOH = 0.1500 x
สมมติความเข้มข้นเริ่มต้นของ HA = X โมล/ลิตร
HA + NaOH
จำนวนโมล HA : NaOH = 1 : 1
เพราะฉะนั้นจำนวนโมล HA = 0.1500 x
= X(
X(
X = 0.048
ความเข้มข้นเริ่มต้น = 0.048 โมล/ลิตร
เพราะฉะนั้นความเข้มข้นของ NaA = 0.048 โมล/ลิตร
การไทเทรตกรดอ่อนกับเบสแก่ที่จุดยุติ มี NaA ซึ่งแตกตัวให้ A-
A- (aq) + H2O (l)
ความเข้มข้นเริ่มต้น 0.048 0 0
ความเข้มข้นที่เปลี่ยนไป -x +x +x
ความเข้มข้นที่ภาวะสมดุล 0.048-x x x

5.88 x 10-9 =
1.4 x 10-5 =
x = 1.68 x 10-5 = [OH-]
pOH = -log[OH-] = -log[1.68 x 10-5] = 4.77
pH = 14 - pOH = 14 - 4.77 = 9.22
ดังนั้น ควรใช้ฟีนอล์ฟทาลีนเป็นอินดิเคเตอร์
สารละลายบัฟเฟอร์ (Buffer Solution)
สารละลายบัฟเฟอร์(buffer solution)หมายถึงสารละลายของกรดอ่อนกับเกลือของกรดอ่อนหรือคู่เบสของกรดอ่อน หรือหมายถึงสารละลายของเบสอ่อนกับเกลือของเบสอ่อน
หรือคู่กรดของเบสอ่อนนั้น สมบัติของสารละลายบัฟเฟอร์ คือ รักษาสภาพ pH ของสารละลายเอาไว้โดยจะเกิดการเปลี่ยนแปลงน้อยมากเมื่อเติมกรดแก่หรือเบสแก่
จำนวนเล็กน้อยลงไปการเตรียม ทำได้โดยการเติมกรดอ่อนลง
ในสารละลายเกลือของกรดอ่อน หรือการเติมเบสอ่อนลงในสารละลายเกลือของเบสอ่อน
ตัวอย่างสารละลายบัฟเฟอร์ เช่น
1.บัฟเฟอร์ของกรดอ่อนกับคู่เบสของกรดอ่อน(เกลือ)
เช่น CH3COOH/CH3COONa มี pH <7
2.บัฟเฟอร์ของเบสอ่อนกับคู่กรดของเบสอ่อน(เกลือ)
เช่น NH3OH/NH4Cl มี pH >7
การคำนวณเกี่ยวกับบัฟเฟอร์
1. pH = Pka + log [salt]/[Acid]
2. pOH=Pkb +log[salt]/[Base]
ตัวอย่าง
1. จงคำนวณหา pH ของสารละลาย 1.00M CH3COOH และ
1.00M CH3COONa(Ka ของ CH3COOH=1.8x10-5 ที่ 25 0C)
วิธีทำ CH3COONa(s)— CH3COO - (aq) + Na +(aq)
CH3COOH + H2O= CH3COO - + H3O +
ความเข้มข้นเริ่มต้น 1.00 1.00 -
ขณะเปลี่ยนแปลง -x +x +x
ที่สมดุล 1.00-x 1.00+x +x
Ka =[ CH3COO - ][ H3O+]/[ CH3COOH ]
1.8x10-5 = x(1.00)/1.00
x =[ H3O+] =1.8x10-5
pH =-log[ H3O+]
=-log(1.8x10-5) = 4.74
2. เมื่อเติม 0.02M OH- ลงในสารละลาย ในข้อ 1 pH จะเป็นเท่าใด
วิธีทำ CH3COOH + OH- =CH3COO - + H2O
เมื่อเริ่มต้น 1.00M 1.00M
เติมเบส 0.02M
ขณะเปลี่ยนแปลง -0.02 M -0.02M +0.02M
หลังจากปฏิกิริยา 0.98M ~0M 1.02M
pH = Pka+ log [CH3COO - ]/[ CH3COOH ]
=-log(1.8x10-5) +log(1.02/0.98)
= 4.77
3.เมื่อเติม 0.02M H3O+ ลงในสารละลายข้อ 1 pH จะเป็นเท่าใด
CH3COO - + H3O+ =CH3COOH + H2O
เมื่อเริ่มต้น 1.00M 1.00M
เติมกรด 0.02M
ขณะเปลี่ยนแปลง -0.02M -0.02M +0.02M
หลังจากปฏิกิริยา 0.98M ~0M 1.02M
pH = Pka+ log [ CH3COO-]/[ CH3COOH ]
=-log(1.8x10-5) +log(0.98/1.02)
= 4.72
